Учёные из Северо-западного научно-технического университета сельского и лесного хозяйства (кит. 西北农林科技大学) вывели трансгенных коров с повышенной устойчивостью к туберкулёзу. Они использовали модифицированную версию CRISPR, благодаря чему им удалось избежать распространённой проблемы исходной технологии — появления незапланированных мутаций. Результаты работы опубликованы в журнале Genome Biology.
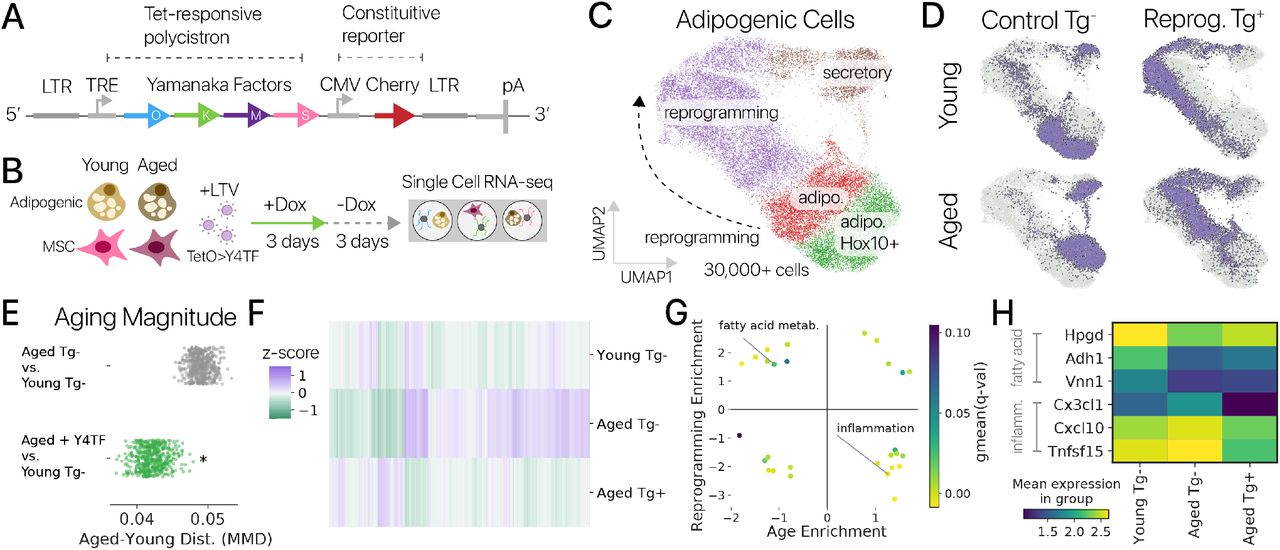
«Мы успешно встроили ген устойчивости к туберкулёзу под названием NRAMP1 в геном коровы благодаря новой версии системы CRISPR — CRISPR/Cas9n, — рассказывает ведущий автор исследования, доктор Юн Чжан (Yong Zhang). — Затем нам удалось вывести коров с повышенной устойчивостью к туберкулёзу. Важно отметить, что наш метод не приводит к появлению нецелевых эффектов, а это значит, что использованная нами технология CRISPR может лучше подойти для создания трансгенного скота с целенаправленно изменённым геномом».
В последнее время в генной инженерии активно применяют технологию CRISPR/Cas9. Она относительно простая, но периодически приводит к возникновению неожиданных мутаций. Предотвратить их появление — одна из самых важных задач современной генетики. «При встраивании в геном млекопитающего нового гена, сложность заключается в том, чтобы найти наилучшее место для его вставки, — объясняет Чжан. — Вам нужно перерыть геном в поисках региона, который, как вам кажется, оказывает наименьшее влияние на другие гены, которые находятся в непосредственной близости. Нам удалось идентифицировать наиболее подходящий для вставки гена участок, который, как мы смогли продемонстрировать, не приводит к возникновению нецелевых эффектов».
Около десяти лет назад стало известно, что развитие и течение туберкулёза регулирует ген NRAMP1. Микобактериями туберкулёза заражён примерно каждый третий житель планеты, но у большинства возбудители находятся в «спящем состоянии». Аллели (варианты) гена NRAMP1 влияют на то, разовьётся ли у человека (или животного) туберкулёз и с какой скоростью будет протекать процесс, если это всё же случится. Исследователи встроили нужный вариант гена NRAMP1 в геном фибробластов, полученных из плодов возрастом 35—40 дней, а затем перенесли ядра этих клеток в яйцеклетки коровы. Из них в лаборатории получили эмбрионы, которые поместили в матки коров. Аналогичные эксперименты провели с использованием классической технологии CRISPR/Cas9, чтобы сравнить результаты.
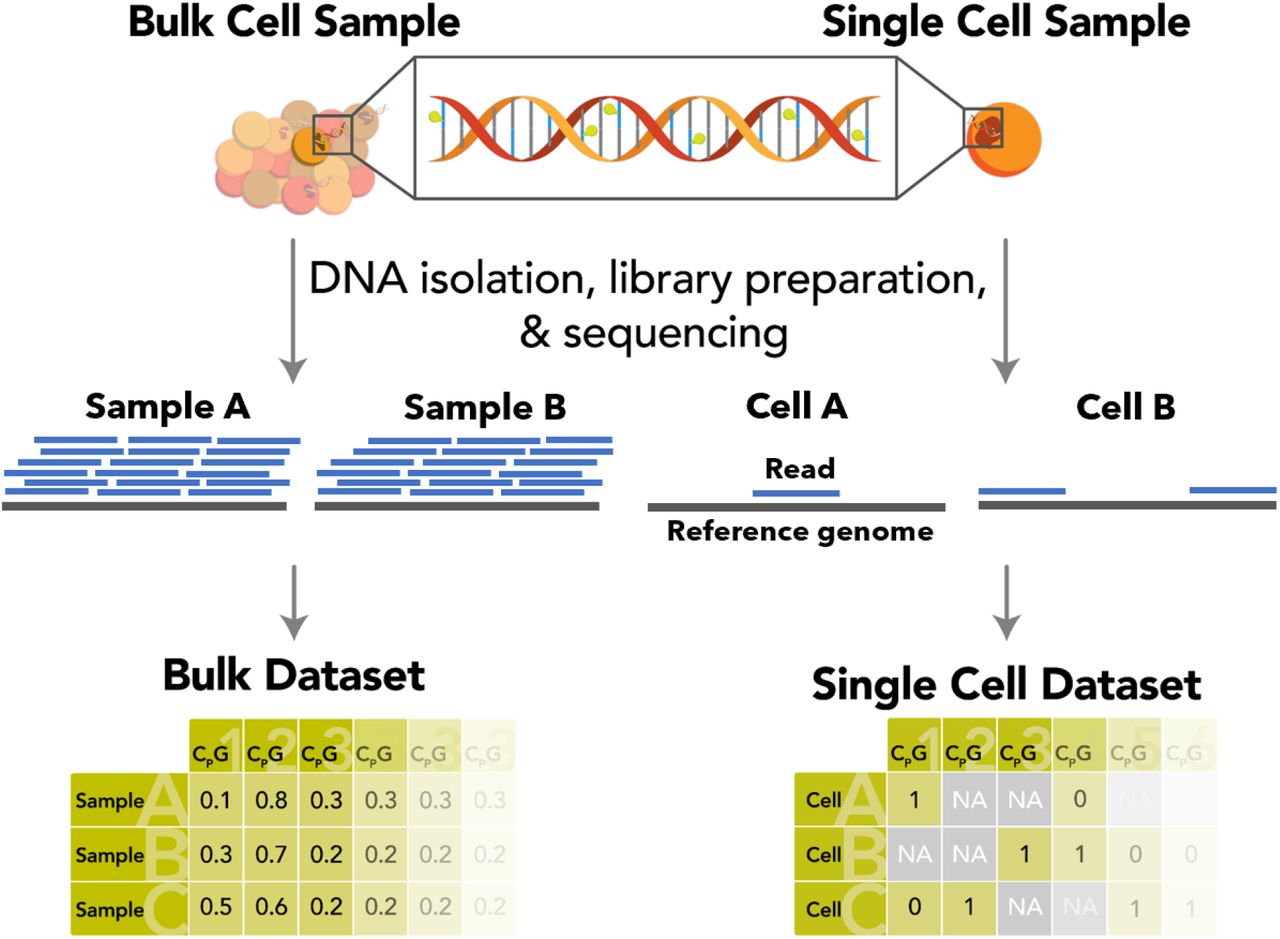
Всего учёные получили из 4819 эмбрионов 20 телят, при этом 11 из них прожили дольше трёх месяцев. Геном выживших телят проверили на наличие непредвиденных изменений с помощью ПЦР и Саузерн-блоттинга — метода, который позволяет обнаружить специфические формы ДНК в клетках. В процессе Саузерн-блоттинга молекулы ДНК удаляют из клеток и специальными ферментами разделяют на небольшие фрагменты. Эти фрагменты отделяют друг от друга, и с помощью генного зонда (меченого радиоактивным веществом участка ДНК) ищут идентичные участки ДНК. Ни у одного из девяти телят, полученных с помощью CRISPR/Cas9n, не удалось обнаружить никаких нецелевых изменений генома. Встроенный NRAMP1 не повлиял на работу других генов, а кодируемый им белок не попал в кожу, мускулы, сердце, печень, почки или лёгкие — а потому учёные заключили, что ген встал точно на место. А вот у двух животных, созданных с помощью CRISPR, незапланированные мутации нашлись.
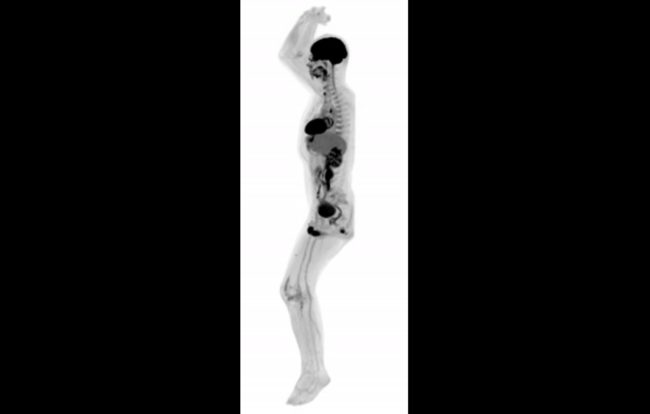
Учёные взяли образцы крови у трансгенных и обычных коров той же породы и подвергли их воздействию возбудителей «бычьего туберкулёза» — микобактерии Mycobacterium bovis. Оказалось, что белые кровяные тельца ГМ-коров борются с инфекцией лучше. В частности, заразившись, клетки трансгенных животных самоуничтожаются в два раза чаще — этот процесс, называемый «апоптозом», помогает предотвратить распространение инфекции. Затем исследователи провели эксперимент in vivo: они случайным образом отобрали шесть трансгенных и столько же нормальных животных и заставили их вдохнуть M. bovis. После этого у телят через определённые промежутки времени брали анализы крови. Измеряя уровень стандартных маркеров инфекции в образце крови, учёные пришли к выводу, что ГМ-коровы действительно более устойчивы к болезни.
«Наше исследование впервые показало, что систему CRISP/Cas9n можно использовать для создания трансгенного скота, не получая при этом нецелевых эффектов, — говорит Чжан. — В ходе экспериментов мы обнаружили участок в геноме коров, в который благодаря этой технологии можно будет вставить новые гены, полезные для сельскохозяйственных животных».
1.02.2017 Источник: 22century.ru