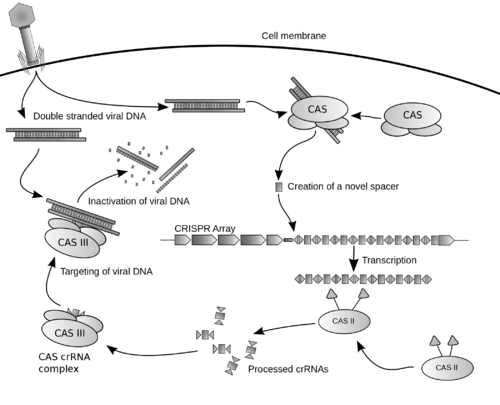
Диаграмма, иллюстрирующая возможный механизм CRISPR.
Короткие палиндромные повторы, регулярно расположенные группами (англ. CRISPR — Clustered Regularly Interspaced Short Palindromic Repeats) — это прямые повторы и разделяющие их уникальные последовательности в ДНК бактерий и архей, которые совместно с ассоциированными генами (Cas, англ. CRISPR-associated genes) обеспечивают защиту клетки от чужеродных генетических элементов (бактериофагов, плазмид). CRISPR-кассеты обнаружены в геномах многих бактерий и большинства архей[1]. Повторы имеют длину от 24 до 48 пар нуклеотидов; они имеют бивалентную симметрию (англ. dyad symmetry), но, как правило, не являются истинными палиндромами. Повторы разделены вариабельными участками ДНК, спейсерами, примерно одинаковой длины. Спейсеры соответствуют по нуклеотидной последовательности определённым фрагментам ДНК чужеродных генетических элементов (протоспейсерам). В связи с этим было предположено и затем показано, что последовательности, разделяющие повторы, происходят из последовательностей геномов бактериофагов, и, соответственно, обеспечивают защиту клеток от инфекций.
Роль в генетической регуляции эндогенных бактериальных генов
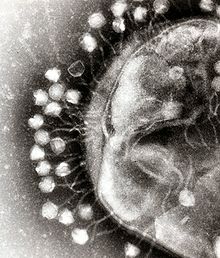
Электронная микрофотография множества бактериофагов, прикрепившихся к бактериальной клеточной стенке
Патогенные и синантропные бактерии содержат большое количество белка Cas9 (англ. CRISPR-associated 9). Было показано, что система CRISPR/Cas может активно участвовать в регуляции эндогенных бактериальных генов, в частности, при взаимодействии бактерий с эукариотическим организмом, в котором они паразитируют. Например, белок Cas9 из Francisella novicida использует уникальную, CRISPR/Cas-ассоциированную малую РНК (scaRNA) для подавления эндогенного транскрипта мРНК, кодирующего бактериальный липопротеин, что позволяет ей ослабить иммунный ответ хозяина и повысить её вирулентность[3].
Методы генной инженерии, базирующиеся на системе CRISPR/Cas9
Разработаны способы высокоизбирательного активирования[4] и ингибирования генов[5], базирующиеся на системе CRISPR/Cas9 (CRISPR-системе II типа)[6][7][8][9][10][11][12][13]. Основными компонентами CRISPR-системы II типа являются CRISPR-кассета, на основе которой синтезируются направляющие crРНК (англ. CRISPR RNA), нуклеаза Cas9 (Csn1) и tracrРНК (англ. trans-activating crRNA), необходимая для процессинга направляющей РНК[1][14][15]. Для направленного редактирования генома эукариотических клеток используют Cas9 Streptococcus pyogenes, Streptococcus thermophilus, Neisseria meningitidis[16][17], а также Cas9 из Staphylococcus aureus (SaCas9), которая на 25 % меньше по размерам, что позволяет упаковывать ее в аденоассоциированный вирус (AAV) для доставки вектора в клетки живого организма, в качестве терапевтического средства[18][19][20]. Происхождение фермента накладывает некоторые ограничения на выбор ДНК-мишеней: например при использовании Cas9 S. pyogenes в качестве мишеней можно выбирать только последовательности, за которыми следует 5'-NGG (где N — любой нуклеотид). Перед использованием в генетических конструкциях ген Cas9 должен быть предварительно оптимизирован по используемым кодонам в соответствии с организмом, геном которого предполагается модифицировать[14].
С целью упрощения манипуляций с клонированием лентивирусных или ретровирусных векторов доставки, crРНК и tracrРНК объединяют в одну цельную РНК (sgРНК) — так называемый «all-in-one CRISPR-Cas9 cloning vector».[21] Это позволяет облегчить конструирование и клонирование серии векторов доставки отличающихся только по пришитой к tracrRNA цепочке «гидРНК», узнающей комплементарную ей, последовательность ДНК, выбранную в геноме по заказу исследователя[22].
Разработана также технология самоклонирующейся CRISPR / Cas9, позволяющая вообще обойтись без клонирования, а использовать короткую двухцепочечную ДНК с последовательностью, кодирующей желаемый локус, и плазмиду, несущую саморасщепляющуюся палиндромную sgРНК. Это позволяет сократить время на подготовку эксперимента всего до двух часов, а его стоимость уменьшить в шесть раз[23]
Модификация ДНК-связывающего домена Cas9 и его слияние c различными регуляторными доменами позволяет получить избирательно направляемые на нужные участки генома с помощью РНК-гидов искусственные факторы транскрипции (crisprTF) и эффекторы[24], искусственные эндонуклеазы рестрикции[25][26], репрессоры, а также ферменты, модифицирующие эпигеном, такие как ДНК-метилазы, деметилазы и гистонацетилтрансферазы, что позволило избирательно регулировать активность определенных генов[27]. Кроме того найдены аналоги Cas9, которые способны расщеплять вместо ДНК молекулы РНК, что позволит редактировать или избирательно подавлять активность микроРНК[28][29]. Так, например, Cas9 из грамотрицательной бактерии Francisella novicida (FnCas9) может быть перепрограммирован так чтобы нацелить его на РНК геном вируса гепатита C, что приводит к ингибированию синтеза вирусного белка в эукариотических клетках[30]. На основе этой системы можно создать сотни средств для обороны против различных вирусов.
Метод сайт-селективного редактирования генома с помощью фермента, узнающего необходимую последовательность цепи ДНК «по наводке» комплементарного ей РНК «гида», обещает революционные перемены в исследованиях и лечении целого ряда заболеваний, от рака[31] и неизлечимых вирусных болезней до наследственных генетических расстройств вроде серповидноклеточной анемии и синдрома Дауна[32]. Он позволил удешевить, упростить и ускорить разработку генномодифицированных микроорганизмов[33], растений[34][35] и домашнего скота, а также поможет разработке генной терапии наследственных заболеваний у человеческих эмбрионов[36][37]. Так, например, технология, разработанная Editas, позволяет изъять клетку из тела живого организма, заменить определенные участки ДНК, а затем вернуть клетку на прежнее место. Предполагается, что таким образом можно запустить процесс лечения некоторых типов заболеваний[38].
Методы исследования, базирующиеся на системе CRISPR/Cas9
Прикрепив к белку Cas9, дефектному по эндонуклеазной активности, зелёный флуоресцентный белок EGFP, можно получить инструмент для визуализации геномных последовательностей в живых клетках млекопитающих и визуального определения длины теломер хромосомы, а также отслеживать динамику генных локусов в течение клеточного цикла.
|
|
НОВОСТИ CRISPR: