|СЕРДЕЧНО-СОСУДИСТАЯ СИСТЕМА| |СЕРДЦЕ| |СОСУДЫ| |КРОВЬ|
|КРОВЬ - ОБЩАЯ ИНФОРМАЦИЯ| |ОРГАНЫ КРОВЕТВОРЕНИЯ| |ДИАГНОСТИКА КРОВИ| |БОЛЕЗНИ КРОВИ| |ВОССТАНОВЛЕНИЕ КРОВИ|
КОМПОНЕНТЫ КРОВИ ГРУППА КРОВИ РЕЗУС-ФАКТОР ДОНОРСТВО
РЕГЕНЕРАЦИЯ КРОВИ
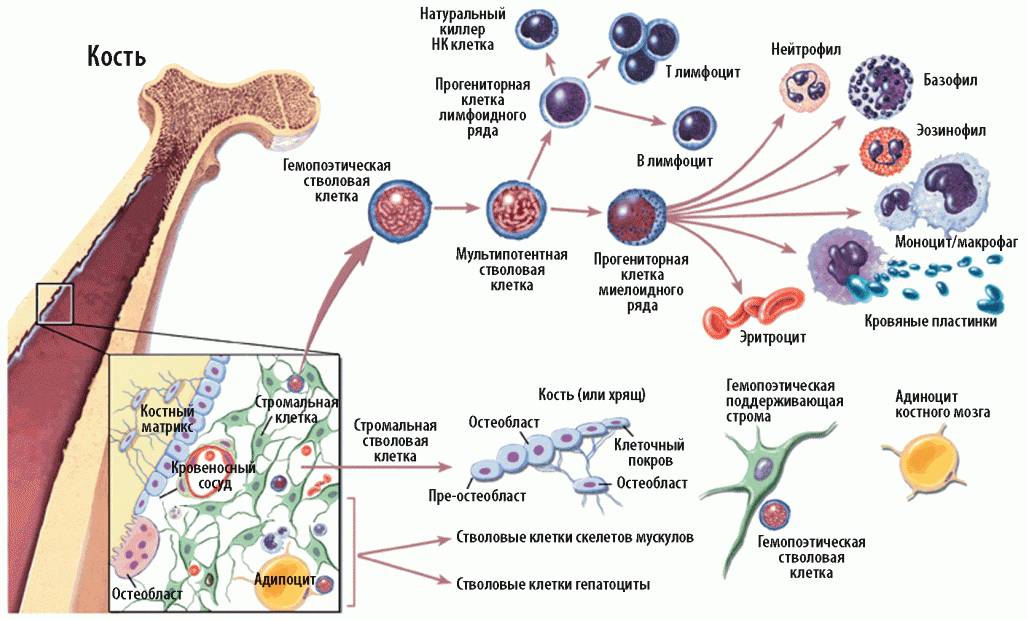
Стволовая клетка крови - первая тканеспецифичная стволовая клетка. Это открытие было сделано русским ученым Александром Александровичем Максимовым (1864 - 1928). Наблюдая за процессами кроветворения, он предположил, что все типы клеток крови происходят из одной клетки-родоначальницы, которая специализируется под действием сигналов, получаемых из крови или других тканей организма. В 1908 году на съезде гематологического общества в Берлине именно он предложил называть такие клетки-родоначальницы "стволовыми ". Гораздо позже, уже в середине 20 века, концепция Максимова о существовании кроветворной стволовой клетки получила экспериментальное подтверждение канадскими учеными Тилл (Till, J.E.) и Маккулох (McColloch E.). Стволовая клетка крови (гемопоэтическая) располагается в красном костном мозге губчатых костей (грудина, гребень подвздошной кости). Как и многие другие тканеспецифичные стволовые клетки, она располагается в специальных нишах. Было выявлено, по крайней мере, 2 ниши для гемопоэтических стволовых клеток в костном мозге, в которых они находятся. Одна из ниш располагается на границе кости и костного мозга и образована остеобластами с которыми контактируют гемопоэтические стволовые клетки. Предполагается, что в таких нишах гемопоэтические стволовые клетки находятся в состоянии покоя и представляют собой некий резервный пул. Также было обнаружено расположение стволовых клеток крови вблизи капилляров костного мозга (так называемая эндотелиальная ниша). Считается, что гемопоэтические стволовые клетки способны быстро активизироваться в ответ на такие стимулы как обширная кровопотеря, физические нагрузки, длительная нехватка кислорода, воспаление и т.п. При этом происходит деление этих клеток и их дифференцировка в направлении лимфоцитов или миелоцитов. Оказалось, что деление гемопоэтической стволовой клетки - не частый процесс, активно делятся уже частично дифференцированные клетки, постепенно специализируясь и образуя все типы клеток крови. Кроветворные стволовые клетки в настоящий момент являются наиболее часто используемыми стволовыми клетками в терапии. Хорошие результаты дает пересадка кроветворных стволовых клеток при разных формах рака крови, когда опухолевый процесс затрагивает собственные стволовые клетки пациента. Врачи сначала удаляют собственные дефектные клетки, а затем пересаживают донорские кроветворные стволовые клетки с помощью трансплантации костного мозга. Такие операции проводят уже более 50 лет. Усовершенствованные технологии, направленные на сбор кроветворных стволовых клеток, в настоящее время используются для лечения лейкемии, лимфомы и некоторых наследственных заболеваний крови.
«Выращивание» крови
Производство молодой крови для трансфузии является одним из путей использования ИПСК.
Известно, что даже одноразовое переливание молодым мышкам крови от старых животных приводит к тому, что у них быстро снижается нейрогенез в гиппокампе, а также наблюдаются некоторые другие дегенеративные изменения и активация воспалительных процессов [[77]]. Это свидетельствует о том, что в старой крови присутствуют факторы, способствующие старению, тогда как молодая кровь омолаживающее действует на мозг (см. рис ниже). Известно также, что терапия с использованием обогащенной тромбоцитами плазмы крови от молодых доноров позволяет восстановить менструальный цикл у женщин, у которых до этого не было месячных уже в течение пяти лет [[78]]. Помогали внутрисуставные инъекции обогащенной тромбоцитами плазмы лечить также остеоартрит коленного сустава. Но только если пациенты были не старше 80 лет [[79]].
Предполагается использовать плазму крови от молодых доноров и для лечения такого старческого недуга как болезнь Альцгеймера [[80]].
Зная, какие белковые факторы способствуют омоложению организма, можно организовать их производство с помощью клеточных культур CAP-Go фирмы CEVEC, которые легко размножаются и способны продуцировать рекомбинантные гликозилированные белки плазмы крови [[81]]. Вместе с тем, зная какие факторы старой крови вызывают старение у молодых, можно разработать способы очистки крови от этих неблагоприятных факторов.
Например, от таких токсичных белков как хемокин CCL11(C–C motif chemokine 11), также известный как эотаксин [[82]]. Уровень этого белка в плазме крови коррелирует со снижением нейрогенеза у старых мышей. Повышение уровня CCL11 у молодых мышей in vivo ведет к снижению нейрогенеза и нарушениям памяти, а также способности к обучению. Увеличен уровень хемокина CCL11 и в плазме крови и спинномозговой жидкости у пожилых людей [ [83]]. Кроме того, этот хемокин – аттрактант избирательно привлекающий эозинофилы, участвует в механизмах развития таких эозинофильных воспалительных заболеваний как атопический дерматит, аллергический ринит, астма и паразитарные инфекции. Некоторые изоформы этого белка являются фактором риска ишемического и гемморагического инсульта [[84]].
Очистить кровь от подобных токсинов может помочь проточный магнитный сепаратор и покрытые моноклональными антителами магнитые микрошарики [[85]].
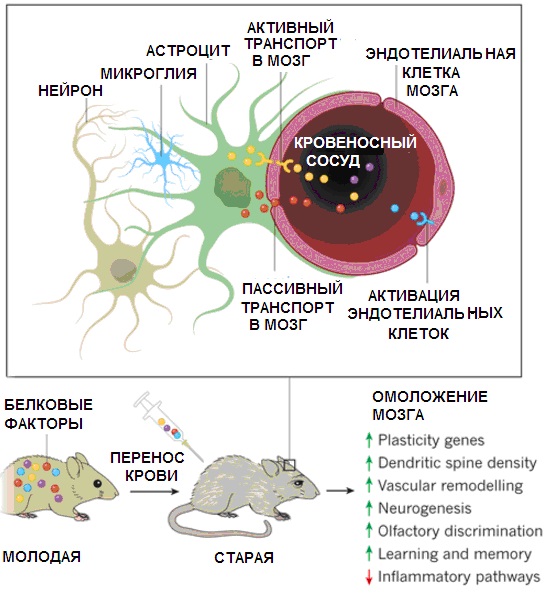
Омоложение мозга старого животного молодой плазмой крови, обогащенной тромбоцитами [[86]]
Следует однако заметить, что вышеописанные технологии получения омолаживающих факторов культивированием клеточных культур и получения омолаживающих факторов культивированием клеточных культур и получение моноклональных антител, используемых для очистки крови с помощью сепаратора, очень дорогостоящее занятие. Поэтому куда дешевле использовать молодую донорскую кровь. Только вот где взять столько доноров, согласных поделиться своей кровью?
Острая нехватка донорской крови побуждает исследователей искать альтернативную замену.
В будущем одним из источников молодой человеческой донорской крови может стать кровь человека, выращенная в организме крупного одомашненного животного, такого как слон, верблюд, корова, лошадь или свинья. Пока для опытов по выращиванию человеческой крови используют гуманизированных мышей с функциональной иммунной системой человека. Для получения гуманизированных мышей лабораторным мышкам линии с иммунодефицитом трансплантируют ткань человеческого тимуса, а также гемопоэтические стволовые клетки, взятые от одного и того же донора. Кроме того, для достижения оптимального приживления трансплантированных человеческих кроветворных стволовых клеток этим мышкам дополнительно внедряют природную мутацию рецептора Kit, в результате которой они теряют способность производить собственные предшественники гемопоэтических стволовых клеток [[87] [88]].
Опыты с гуманизированными мышками линии NSGW41 показали, что эритро-мегакариоцитарные клетки человека хорошо приживаются в организме этих мышей; факторы роста, ответственные за пути дифференциации человеческих клеток, совместимы между видами и позволяют достичь in vivo полного созревания тромбоцитов человека, а также получить содержащие ядро клетки-предшественники человеческих эритроцитов. В крови животного, однако, эти клетки не накапливались, поскольку их тут же уничтожали макрофаги [[89]]. Очевидно, необходимо модифицировать и макрофаги. Аналогичные эксперименты вскоре можно будет воспроизвести на мутантных поросятах, у которых либо нет тимуса, либо он не развит [[90]]. C мутантными поросятами, однако сложность в том, что они в случае иммунодефицита, теряют способность к воспроизводству потомства и крайне подвержены вирусным инфекциям, которые трудно лечить. Одна надежда на слонов, но их пока никто не исследует на предмет модификации их иммунной системы для «гуманизации» и толерантности к клеткам человека – слишком дорогой объект для опытов, пусть и жизненно необходимых человечеству.
Упростить трансплантацию человеческих гемопоэтических клеток может новый способ «расчистки» ниши для этих клеток в организме животного. Оказалось, что если продержать животное 1-2 недели на диете без незаменимой аминокислоты – валина, то его гемопоэтические клетки гибнут, высвобождая место для человеческих гемопоэтических клеток [[91]].
НОВОСТИ КРОВИ