В век инноваций мы все чаще встречаем заголовки в стиле «Сенсация! Ученые вырастили сердце из стволовых клеток» или «Впервые в лаборатории были выращены работающие легкие». Самое «прекрасное» название статьи появилось около года назад: «Ученые вырастили взрослый мозг в пробирке». К сожалению, далеко не все заявленные «плоды клеточной агрономии» можно действительно считать полноценными и готовыми к терапевтическому использованию. Но наука не стоит на месте, с каждым днем всё активнее приближаясь к созданию чего-то революционного. Как же разобраться, что действительно вскоре станет рутинной процедурой, а что – только первые шаги к будущему?
Начнем с терминов
«Выращивание» – именно так чаще всего называют создание органов вне организма. Можно провести простейшие аналогии: клетки (зернышки) садят на специальные матриксы-каркасы (в почву) и создают нужное химическое окружение с помощью разных веществ (удобряют). Но всё не так просто. Для создания, например, печени нам понадобятся очень разные «зерна», так как этот сложный орган состоит из разных типов клеток с различными потребностями. «Почва» подойдет тоже не всякая и, кроме того, её не достаточно просто высыпать в горшок. Прежде чем «садить зерно», почве нужно придать форму, которая будет соответствовать строению органа, а также заселить разные типы клеток в разные участки.
Прежде чем «садить зерно», почве нужно придать форму, которая будет соответствовать строению органа, а также заселить разные типы клеток в разные участки.
«Удобрять» конструкцию нужно очень грамотно, используя правильные дозы и сочетания необходимых веществ: цитокинов, индукторов определенных клеточных превращений, питательных веществ и т.д. Но и это ещё не всё, ведь даже если правильные клетки «дадут всходы» (т.е. прикрепятся, начнут делиться и сформируют нужную ткань), для полноценного функционирования в орган должны будут зайти капилляры с кровью. Этот процесс называется васкуляризация, одна из активно решающихся задач тканевой инженерии. Однако и сосудов для полноценной работы мало, так как необходимы ещё и связи с нервной системой. И это ещё одна важная задача тканевой инженерии – иннервация органов. Впоследствии полученный объект необходимо определённым образом интегрировать с учетом центральной регуляции (нервной, гуморальной и иммунной), и это одна из главных и самых сложных задач.
Вернемся к «зернам»
В тканевой инженерии используют разные клетки – как стволовые, т.е. способные делиться и превращаться в разные типы клеток, так и специализированные, т.е. уже умеющие выполнять какую-то конкретную функцию. Стволовая клетка под влиянием сигнальных молекул (факторов роста, цитокинов) и физических факторов (жёсткость, структура каркаса) может превратиться в нужную для конкретной задачи. Если клетка плюрипотентная, то превратиться она сможет практически во все клетки организма, если мультипотентная – в широкий, но ограниченный происхождением, диапазон типов. Можно использовать и клетки-предшественницы, т.е. ещё не дошедшие до конечной степени специализации. Иногда имеет смысл использовать именно обладающие «богатой фантазией» стволовые клетки, иногда рациональнее выбрать уже определившиеся со своим предназначением специализированные, от которых можно не ждать сюрпризов. Таким образом, всё зависит от конкретной задачи.
Если клетка плюрипотентная, то превратиться она сможет практически во все клетки организма, если мультипотентная – в широкий, но ограниченный происхождением, диапазон типов.
Несколько слов о «почвах»
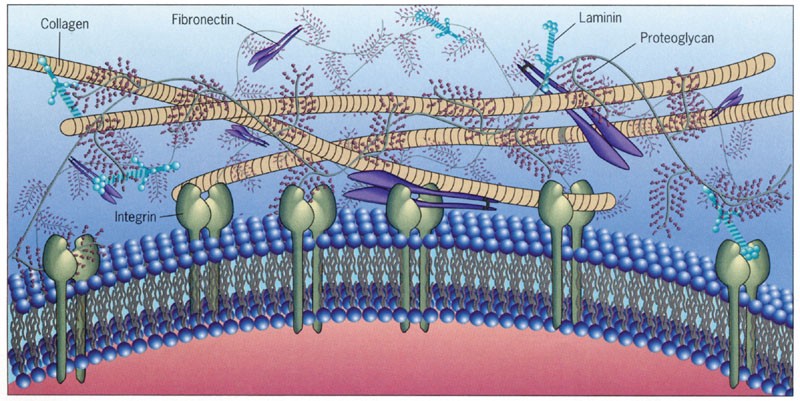
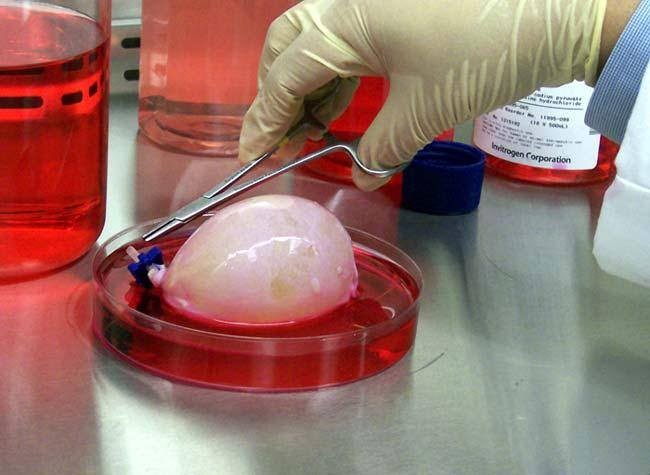
Для создания тканеинженерных конструктов чаще всего используют матриксы из коллагенов разных типов, хитозана, фибрина и многих других веществ, а также из синтетических полимеров, например, полиэтилен гликоля. Некоторые матриксы являются биодеградабельными, т.е. такими, которые сами рассасываются со временем, некоторые – наоборот стойкими. Снова-таки, под разные задачи нужны материалы с разными свойствами. Сформировать нужный конструкт можно разными путями, среди которых один из наиболее обсуждаемых – 3Д-печать. Ещё один вариант создания основы органа – донорский, часто трупный, материал. Одним из самых известных примеров стала трахея. Орган умершего человека очищается от клеток хозяина, вымывается и становится иммунологически условно нейтральным. Оставшаяся основа заселяется клетками человека, которому нужна пересадка трахеи.
В целом, сегодня корректнее говорить скорее о массовом создании определенных тканевых конструкций, а не о непосредственном «выращивании» или полноценной «печати» человеческих органов. Сложность создания органа «под ключ» прямо пропорциональна сложности его строения. Соответственно, такие структуры как хрящ или полые, похожие на трубки, органы, воспроизвести значительно проще, чем мозг или сердце. С трёхмерной печатью непосредственно клетками (т.е. когда речь идет не просто о создании каркаса) дела обстоят ещё более запутанно: в мире есть всего несколько лабораторий, заявляющих, что им удается воплощать в жизнь такую технологию, но во всех случаях это на данный момент уникальная ювелирная работа. Проблемы имеются и в условиях, в которых оказывается печатаемый материал (живая клетка), в процессе производства (температура, давление и многое другое), и в ограничениях размеров, и во всех вышеперечисленных процессах (васкуляризация, иннервация, центральная регуляция).
|
|
И ещё один нюанс
Все описанные манипуляции требуют очень дорогостоящего оборудования, реактивов и высококлассных специалистов. Соответственно, даже самый успешный отчет из одной лаборатории не гарантирует быстрого распространения удачной методики во все уголки мира.
Даже самый успешный отчет из одной лаборатории не гарантирует быстрого распространения удачной методики во все уголки мира.
Поэтому стоит искренне радоваться каждому прорыву и новостям о создании комплексного фрагмента кишечника, и о пересаженных мышкам легких, и о работающих ушных раковинах. Каждый маленький лабораторный прорыв – шаг к персонализированной медицине будущего. Однако думать, что уже завтра подобные процедуры станут массово доступными – всё же слишком наивно. Стоит подождать чуть дольше… Например, до послезавтра.
5.12.2016 Источник: Ольга Маслова, клеточный биолог likar.info