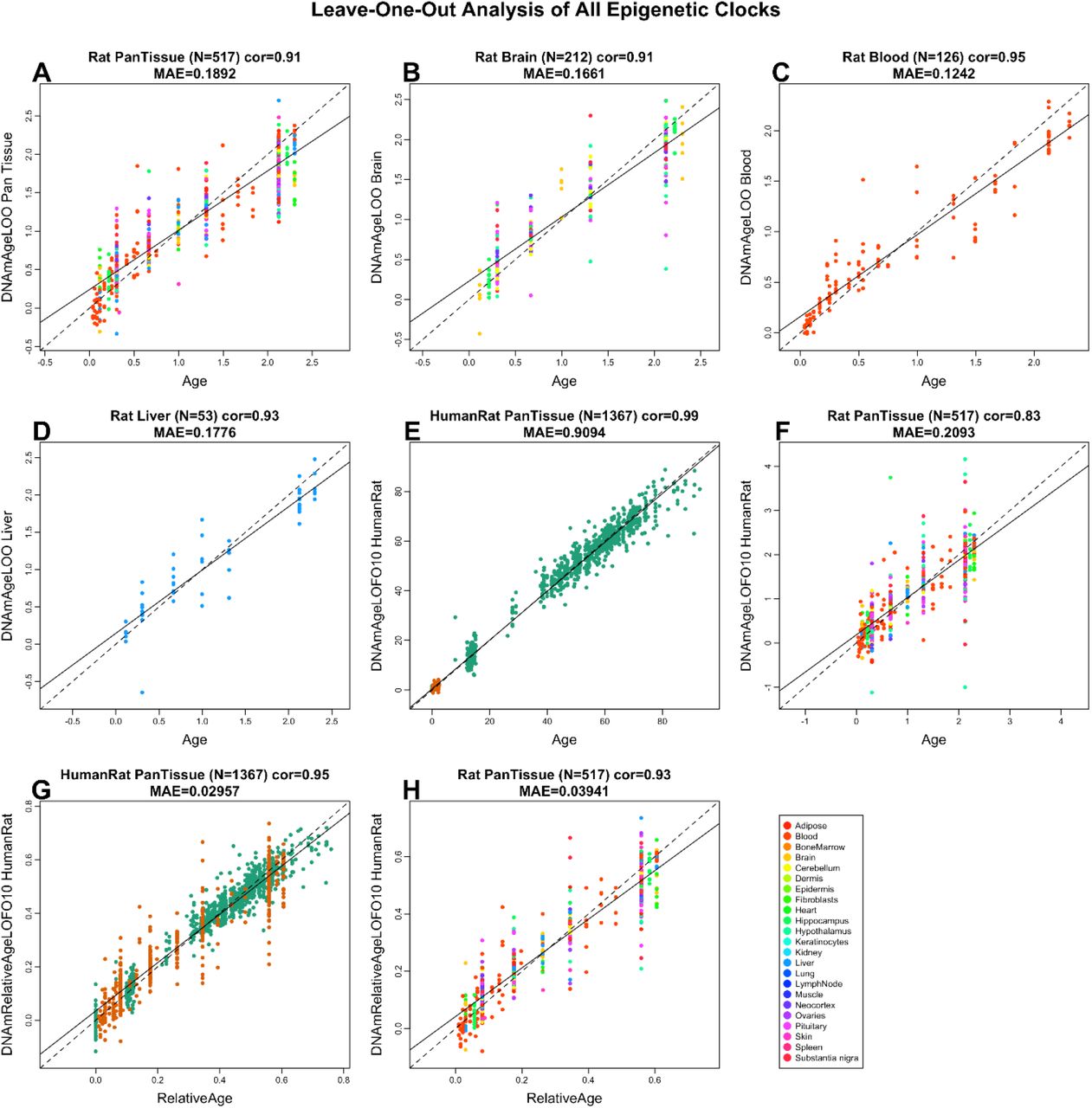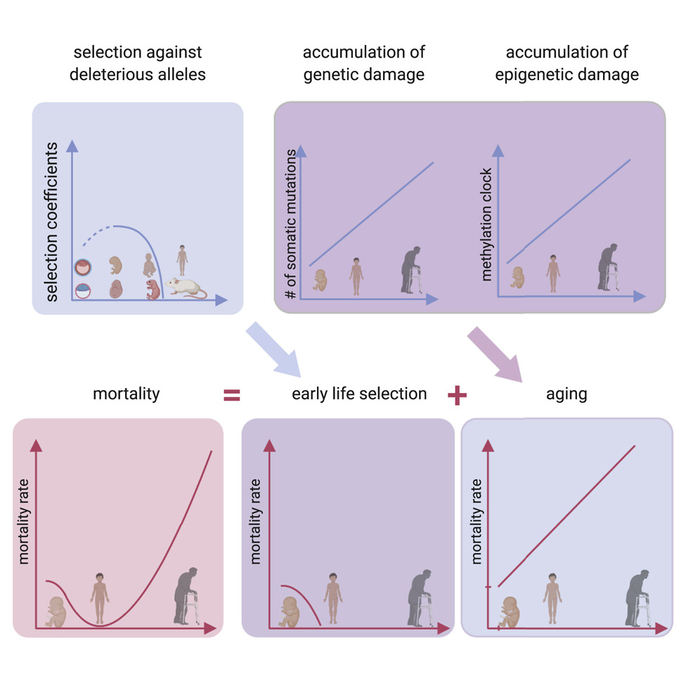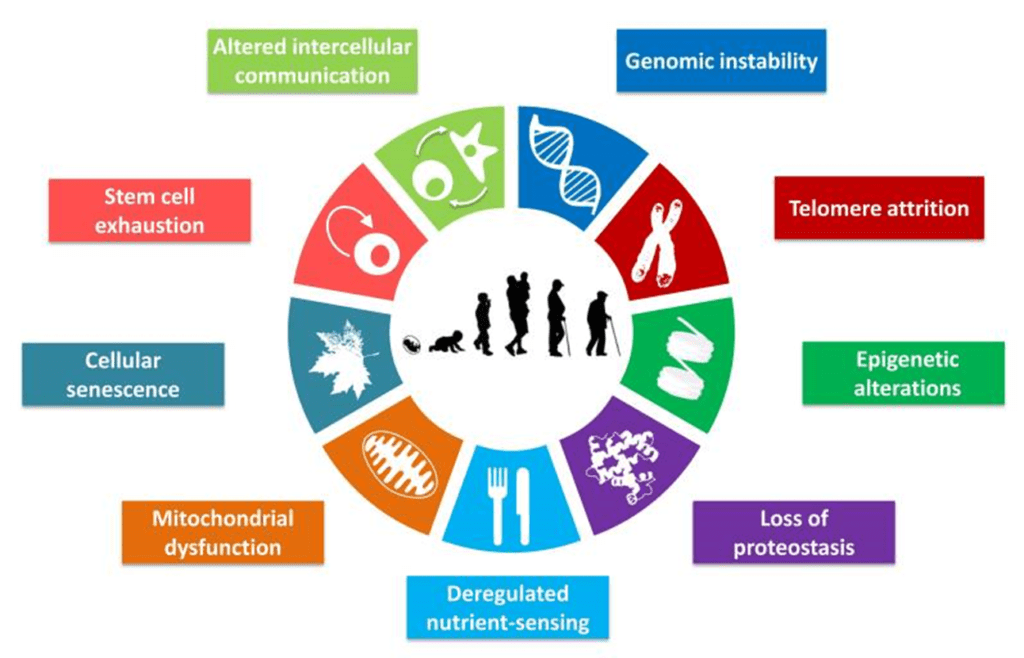
“Если вы не можете измерить это, вы не можете улучшить его”, — так сказал Уильям Томсон, великий ирландский физик известный как лорд Кельвин. B. Vellas и соавторы в своей новой работе предложили свои биомаркеры старения по каждому из 9 общих признаков старения, рассматриваемых в самой значительной работе про старение «Hallmarks of Aging». Вот принцип, которым они руководствовались: «Основываясь на современной литературе, для каждого признака биологического старения мы предложили биомаркер здорового старения. Наш выбор был основан на их связи со смертностью, возрастными хроническими заболеваниями, старческой астенией и / или нарушением функций».
1. Геномная нестабильность. Микроядра
В качестве биомаркера геномной нестабильности авторы предложили микроядра, определяемые микроядерным анализом.
Генетическое повреждение накапливается с возрастом из-за внешних и внутренних факторов. Нестабильность генома возникает в результате дисбаланса между повреждением и восстановлением ДНК. Повреждение хромосом можно оценить с помощью микроядерного анализа, который измеряет разрушение хромосом. Микроядра образуются из фрагментов хромосом, образовавшихся в ходе нарушенного клеточного деления или апоптоза. Увеличение содержания в организме клеток с микроядрами связано со старением, раком, нейродегенеративными заболеваниями, употреблением табака.
www.ncbi.nlm.nih.gov/pubmed/21763453?dopt=Abstract
www.ncbi.nlm.nih.gov/pubmed/21164187?dopt=Abstract
Также исследования показали, что увеличение микроядер связано со старческой астенией (Frailty)
academic.oup.com/biomedgerontology/article/73/7/864/4807480
2. Укорочение теломер
Теломеры представляют собой концевые участки хромосом, которые укорачиваются каждый раз, когда клетки делятся. Это один из наиболее изученных признаков старения, с более чем 8000 публикаций в PubMed на сегодняшний день. Двумя основными методами, используемыми для измерения длины теломер, являются Southern blot (измерение размера ферментативно расщепленных фрагментов теломер) и количественная полимеразная цепная реакция (qPCR).
В недавнем мета-анализе двадцати пяти исследований (Где число исследуемых было n=121749, 21763 умерших) укорочение теломер было предиктором смертности от всех причин.
www.ncbi.nlm.nih.gov/pubmed/30254001?dopt=Abstract
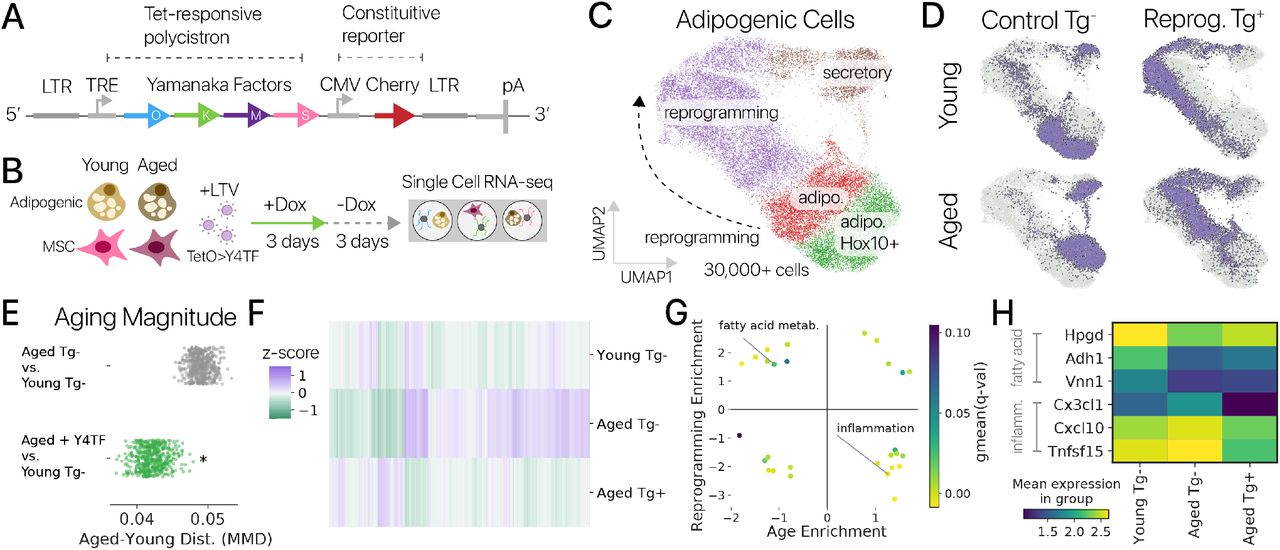
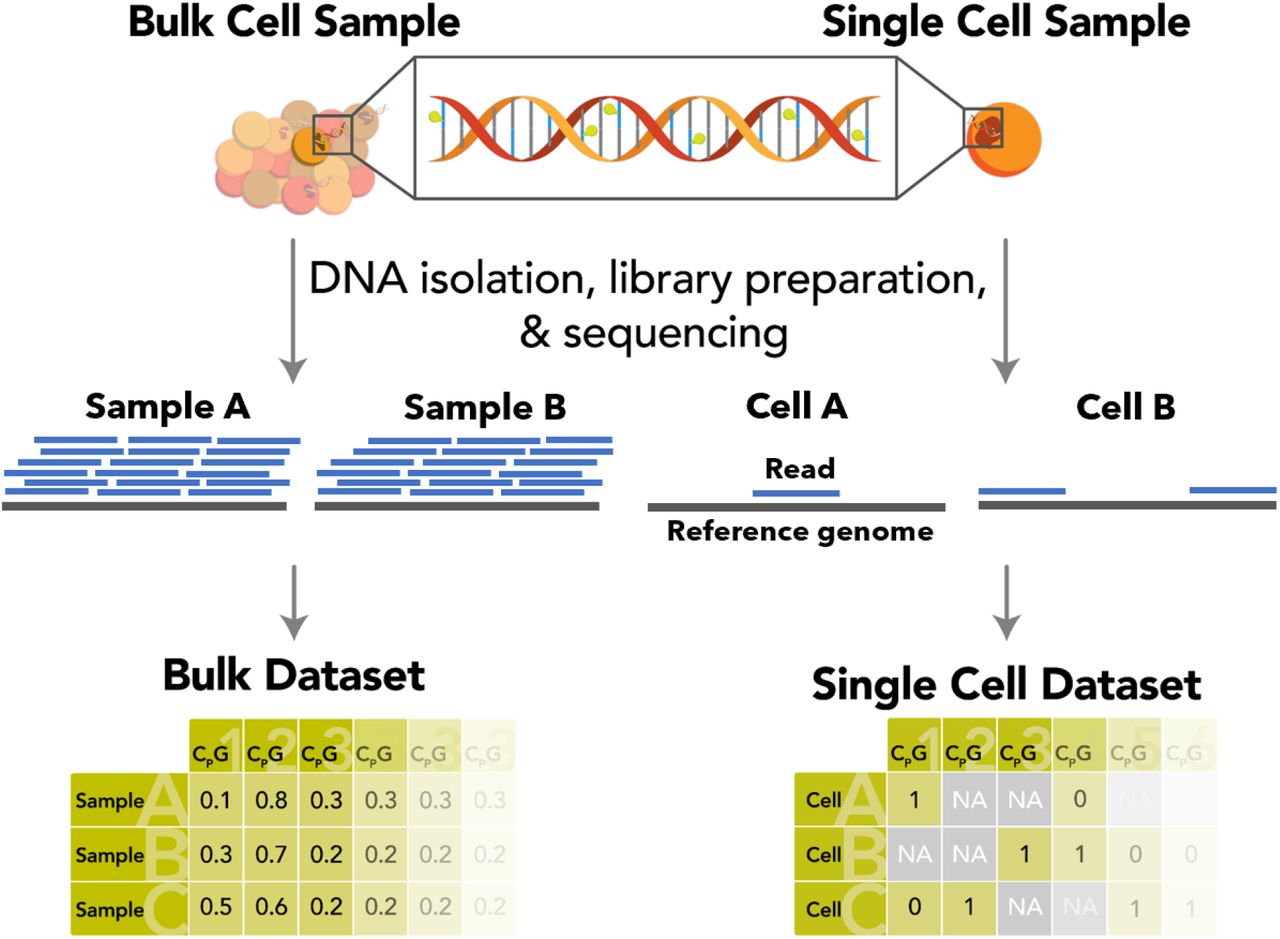
3. Эпигенетические модификации. Часы метилирования ДНК
Изменения в последовательности ДНК — это не единственные возрастные геномные изменения. Эпигенетические модификации, такие как метилирование ДНК, модификация гистонов, ремоделирование хроматина, влияющие на экспрессию генов, также являются особенностями старения. Среди них изменения в метилировании CpG-островков являются основными регуляторами экспрессии генов. На основании этих изменений, относительно постоянных между особями, были разработаны «Эпигенетические часы метилирования ДНК”, которые как утверждают авторы, точно показывают биологический возраст и риск развития возрастных патологий.
4. Нарушение протеостаза. Кластерин
Известно, что внутриклеточный белковый гомеостаз, или протеостаз, поддерживается с помощью нескольких механизмов контроля качества: рефолдинг белка с помощью белков-шаперонов и деградация убиквитин-протеасомной системы или посредством аутофагии. Из-за клеточного стресса, агрегация неправильных белков является признаком старения и связанных с возрастом заболеваний, таких как болезнь Альцгеймера. Белок кластерин (также известный как аполипопротеин J) поддерживает нормальный протеостаз, предотвращая накопление неправильных белков. Несколько исследований показали связь между уровнем кластерина и возрастными заболеваниями. Так, Riwanto описал, что снижение уровня ЛПВП-ассоциированного кластерина связано с ишемической болезнью сердца. www.ncbi.nlm.nih.gov/pubmed/23349247?dopt=Abstract В патогенезе болезни Альцгеймера уровни кластерина напротив возрастают. www.ncbi.nlm.nih.gov/pubmed/20603455?dopt=Abstract
5. Нарушение регуляции питательных веществ. Сиртуины
Помимо инсулина и сигнального пути IGF-1, сиртуины являются другими датчиками питательных веществ с противоположным эффектом: их сигнальный путь связан с дефицитом питательных веществ и катаболизмом. Активация сиртуинов имитирует ограничение калорий и улучшает продолжительность жизни и здоровье. Сиртуин -1 играет центральную роль в выживании и регенерации клеток скелетных мышц, как это было описано Sharples и соавторами. www.ncbi.nlm.nih.gov/pubmed/25866088?dopt=Abstract Сиртуин-1 первоначально был описан как ядерный протеин. Но недавно его обнаружили в сыворотке. В этом исследовании более низкие уровни сывороточного сиртуина-1 были обнаружены у пожилых людей, у пациентов с болезнью Альцгеймера, по сравнению молодыми людьми. www.ncbi.nlm.nih.gov/pubmed/23613875?dopt=Abstract
6. Митохондриальная дисфункция. GDF 15 и Апелин
Старение человека обычно связано с прогрессирующей митохондриальной дисфункцией. Среди важных параметров, участвующих в этой дисфункции, снижение эффективности дыхательной цепи, наблюдаемое при старении, характеризуется повышением продукции активных форм кислорода (АФК), дефектами целостности митохондрий и снижением биогенеза митохондрий (контролируемого, в частности, сиртуинами). GDF-15 — это стресс-индуцированный цитокин и член суперсемейства трансформирующего фактора роста β. GDF-15 рассматривается как диагностический маркер для наследственных митохондриальных заболеваний, и потенциально как маркер митохондриальной дисфункции www.ncbi.nlm.nih.gov/pubmed/27018280?dopt=Abstract Исследования показывают, что апелин, индуцированный физическими упражнениями миокин, также может рассматриваться как предполагаемый биомаркер старения, связанный с митохондриальной дисфункцией. Апелин усиливал мышечную функцию посредством митохондриогенеза, а также других путей, связанных с признаками старения: аутофагии, воспаления и мышечных стволовых клеток. www.nature.com/articles/s41591-018-0131-6
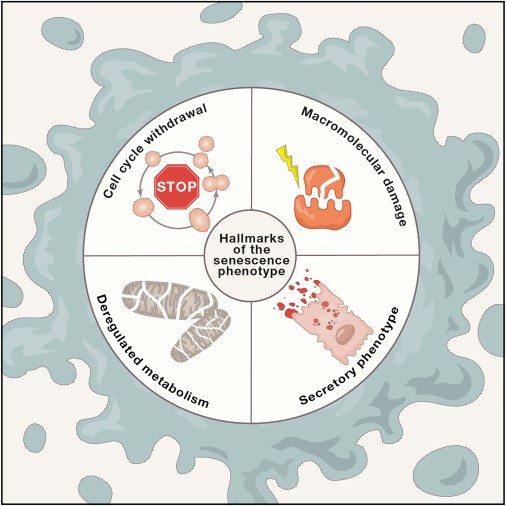
7. Клеточное старение. p16Ink4A
Клеточное старение — это состояние стабильной остановки клеточного цикла в сочетании с фенотипическими изменениями, включая продукцию провоспалительных факторов SASP. SASP способствует воспалению и дисфункции ткани. Появившееся как компенсаторный механизм, направленный на предотвращение пролиферации поврежденных клеток, старение клеток индуцируется разными возрастными стимулами: укорочением теломер, повреждением ДНК и чрезмерной митогенной сигнализацией, в частности белком-супрессором опухоли p16Ink4a, при эпигенетической де-репрессии локуса ink4/ark.
Экспрессия белка p16Ink4A возрастает при старении в различных тканях у животных и человека.
www.ncbi.nlm.nih.gov/pubmed/15520862?dopt=Abstract
onlinelibrary.wiley.com/doi/full/10.1111/j.1474-9726.2006.00231.x
Также показано, что транскрипция p16Ink4a Т-лимфоцитах периферической крови положительно связана с возрастом, употреблением табака, физической активностью и может быть одним из биомаркеров старения.
www.ncbi.nlm.nih.gov/pmc/articles/PMC2752333
Кроме этого, в метаанализе 372 исследований GWAS, направленных на выявление полиморфизмов предрасположенности к возрастным заболеваниям, локус ink4/ark, кодирующий белок p16Ink4a, был связан с самым высоким числом заболеваний, включая болезнь Альцгеймера, сердечно-сосудистые заболевания, рак и сахарный диабет типа 2.
www.ncbi.nlm.nih.gov/pmc/articles/PMC3444649
8. Истощение стволовых клеток: циркулирующие остеогенные клетки-предшественники
Репаративный и регенеративный потенциал многих тканей снижается с возрастом, что связано с функциональным истощением в нескольких пулах стволовых клеток (например, гемопоэтических, нервных, мезенхимальных и кишечных эпителиальных стволовых клеток). Взрослые стволовые клетки присутствуют в каждой ткани и органах после развития и регенерируют поврежденные ткани на протяжении всей жизни. Во время старения функция стволовых клеток снижается. Истощение стволовых клеток рассматривается как интегративное следствие нескольких признаков старения, описанных выше, включая повреждение ДНК, эпигенетические изменения, укорочение теломер, старение клеток и митохондриальную дисфункцию. Но истощение стволовых клеток трудно измерить неинвазивно до наступления его клинических последствий, таких как анемия и цитопении (т.е. клеточный дефицит) для гемопоэтических стволовых клеток, а также саркопения для мышечных стволовых клеток и снижение функции кишечника для кишечных эпителиальных стволовых клеток. До сих пор имеется недостаточно данных о потенциальных биомаркерах этого признака старения. Циркулирующие остеогенные клетки-предшественники были предложены в качестве суррогатного маркера популяции мезенхимальных стволовых клеток в костном мозге. asbmr.onlinelibrary.wiley.com/doi/full/10.1002/jbmr.370 Процент клеток остеогенных клеток-предшественников обратно коррелирован с возрастом. Также более низкие уровни этих клеток были связаны с астенией, более низкой физической работоспособностью (измеряемой силой захвата и скоростью ходьбы) и инвалидностью, независимо от возраста и сопутствующей патологии. academic.oup.com/biomedgerontology/article/71/9/1124/2605419
9. Измененная межклеточная коммуникация: инфламмасомы и IMM-AGE
Старение связано с изменениями в связях между клетками и хроническим воспалением, inflammaging. Это воспаление рассматривается как следствие нескольких признаков старения, описанных выше, в том числе клеточного старения (через SASP) и потери протеостаза, поскольку неправильно свернутые белки представляют собой сигнал опасности, который запускает врожденный иммунный ответ.
Одним из главных путей воспаления является сигнальный путь инфламмасом. Инфламмасома представляет сложную систему внутриклеточных белков, которые собираются при обнаружении сигналов стресса/опасности и запускают созревание и высвобождение провоспалительных цитокинов (интерлейкина-1β и интерлейкина-18). Мышиные модели, лишенные инфламмасомы NLRP3, демонстрируют уменьшение воспаления, непереносимости глюкозы, дегенерации гиппокампа, нейровоспаления.
www.ncbi.nlm.nih.gov/pmc/articles/PMC4017327
У пожилых людей от 60 до 90 лет активация инфламмасом (измеренная по экспрессии генов nlcrc4 и nlrc5 в клетках цельной крови и продукции интерлейкина-1β) была положительно связана с артериальной гипертензией и артериальной жесткостью и отрицательно связана с личным и семейным долголетием.
www.ncbi.nlm.nih.gov/pubmed/28092664?dopt=Abstract
Кристаллы холестерина и β-амилоидные белки могут инициировать сборку воспалительных комплексов инфламмасом, этот путь участвует в прогрессировании атеросклеротического поражения и нейровоспалении при болезни Альцгеймера.
www.ncbi.nlm.nih.gov/pmc/articles/PMC2946640
www.ncbi.nlm.nih.gov/pmc/articles/PMC3812809
Помимо воспаления, immunosenescence включает количественные и функциональные изменения множества факторов как врожденных, так и адаптивных звеньев иммунной системы.
Immunosenescence может усугублять процесс старения, связанный с описанными выше признаками старения, в частности из-за неспособности уничтожать патогенные микроорганизмы, а также предраковые клетки, стареющие клетки и неправильно свернутые белки. A. Alpert и соавторы создали показатель траектории иммунного старения IMM-AGE, на основе которого можно предсказывать риски смертности от всех причин.
www.ncbi.nlm.nih.gov/pmc/articles/PMC6686855
09.02.2020 Источники: https://habr.com/ru/post/487628/
Статья: «Пересмотр признаков старения для выявления маркеров биологического возраста»