Весь XX и XXI век – это, конечно, прежде всего, открытия в генетике, которые во многом определили тренд развития всей медицины.
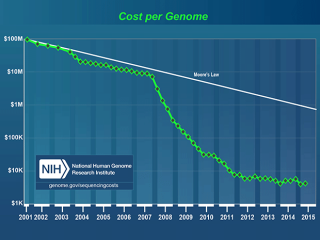
Стоит вспомнить открытие метода секвенирования по Сангеру в 1974 году, проект «Геном человека», который продолжался более 10-ти лет, открытие в начале этого столетия метода секвенирования нового поколения (NGS).
Сейчас в большинстве развитых стран мира генетические исследования стали рутинным методом диагностики в кардиологии и полностью финансируется государством. В нашей стране генетическая диагностика по-прежнему остается дорогостоящим и малодоступным методом, работать с которым готовы далеко не все специалисты.
Но уже сейчас понятно, что это направление в кардиологии будет развиваться, и многие клинические случаи доказывают, насколько оно необходимо.
Холестерин и наследственный холестерин – это разные вещи
О том, что избыточное количество «плохого» холестерина в крови, приводит к развитию атеросклероза, грозит инфарктами и инсультами, знают, наверное, все.
Но современная кардиология говорит о том, чтобы правильно поставить диагноз, определить, каков риск у пациента развития сердечно-сосудистых заболеваний при высоком уровне холестерина (больше 7,5-8 ммоль/л), нужны генетические исследования.
Здесь важно выяснить, есть ли у больного семейная гиперхолестеринемия (СГХС). То есть наследственное заболевание с высоким риском развития сердечно-сосудистых осложнений и большой вероятностью поражения родственников. Если при повышенном уровне холестерина с наследственностью все нормально, тактика лечения одна. Но если с генетикой повезло не очень – то заболевание может протекать совсем по-другому, часто требуется более серьезное лечение.
«Протекать болезнь (СГХС) может бессимптомно, особенно у детей. И если ее не диагностировать вовремя и не лечить, тогда риск развития ишемической болезни сердца увеличивается в 20 раз. А у мужчин, которые не получали лечение, на 50% увеличивается риск фатальных и нефатальных инфарктов миокарда в возрасте до 50 лет. У женщин этот риск на 30% выше в возрасте до 60 лет», - говорит кардиолог, сотрудник научного комитета генетической лаборатории Health in Code (Испания) Наталья Соничева.
Еще один тревожный знак - СГХС может стать причиной 5% остановок сердца у людей моложе 60-ти лет и 20% моложе 45 лет.
Очень важно, что генетический анализ на СГХС может проводиться и у детей, начиная с пяти лет, если у мамы или у папы есть семейная гиперхолестеринемия. Тогда, по современным рекомендациям, врач, если в этом есть необходимость, может назначать статины с 8-10 летнего возраста.
«Наследственных сердечно-сосудистых заболеваний очень много»
Генетические исследования в кардиологии очень важны и при других наследственных сердечно-сосудистых заболеваниях.
«У этих заболеваний одно общее важное свойство – гетерогенная клиника¸ поэтому диагностировать их сложно. Как правило, они семейные, а механизм наследования аутосомно-доминатный – когда в каждом поколении есть заболевшие родственники, половина родственников будут больными», - говорит Наталья Соничева.
Таких наследственных сердечно-сосудистых заболеваний очень много. Если сложить вместе кардиомиопатии, электрические заболевания миокарда, наследственные заболевания аорты и семейную гиперхолестеринемию, которая встречается чаще других, то окажется что в России это примерно 850 тысяч человек.
Диагностировать эти заболевания, безусловно, очень важно именно на раннем этапе, подчеркивает Наталья Соничева, тогда это позволяет назначать правильное лечение.
Медицинский детектив
«Например, в нашей практике был такой клинический случай. Вот такая семья: женщина – 79 лет с артериальной гипертензией, у ее сестры - мерцательная аритмия, инсульт, гипертрофическая кардиомиопатия. Также у сестры есть семнадцатилетняя внучка с совершенно другой клинической картиной, тяжелой симметричной концентрической гипертрофией левого желудочка, а у матери – нет отклонений на ЭхоКГ. То есть, удивительно, что у трех поколений - разная клиника», - говорит Наталья Соничева.
Здесь важно было понять, как лечить девочку. При генетическом исследовании было обнаружено, что вся семья, все три поколения являются носителями мутации в тропонине I, гене, кодирующим белок саркомера. Данная мутация ведет к развитию классической наследственной гипертрофической кардиомиопатии. Получается, если есть одна мутация, то и клиника во всех трех поколениях должна быть похожей. Но клиника-то была совершенно разной.
И тогда с помощью развернутого генетического исследования кардиологи выяснили, что у девочки есть еще вторая мутация в гене, кодирующим белок тирозинфосфокиназу, отвечающую за каскадный комплекс митоген-активируемых протеинкиназ, которые отвечают за пролиферацию, дифференцировку и апоптоз клеток. При нарушениях в этом каскаде развиваются заболевания РАСопатии, такие как синдромы Нунана, Леопарда и тд., требующие абсолютно другой тактики лечения и имеющие более неблагоприятный прогноз.
Генетика помогает предотвратить смерть
Другая причина, по которой нужно проводить генетическую диагностику – это раннее выявление пораженных родственников, т.к. главная угроза всех наследственных кардиоваскулярных заболеваний - это внезапная сердечная смерть, которая может наступить при полном благополучии в молодом возрасте.
«Например, такой клинический случай: в семье два брата, один погибает от внезапной смерти в возрасте 20-ти лет на фоне физической нагрузке, другой брат в 22 года - почти сразу после смерти первого (играя в футбол). В этой семье есть еще и сестра, которой, естественно, просто страшно. Мы провели генетическое исследование и нашли злокачественную мутацию, ведущую к развитию катехоламинергической полиморфной желудочкой тахикардии, где главное осложнение - это внезапная смерть в молодом возрасте на фоне физических упражнений или стресса. В нашей базе данных у нас есть уже информация об этой же самой мутации, которая встречалась в восьми семьях, среди них было 16 внезапных смертей в возрасте до 40 лет. И если бы генетическая диагностика была проведена хотя бы после смерти первого брата, то удалось бы спасти второго пациента просто назначением бета-блокаторов. Девочка, к счастью, не является носителем этой мутации, она полностью здорова. Только на основании генетической диагностики удалось сделать такой вывод», - говорит Наталья Соничева.
Здесь важнее всего интерпретация данных
Генетические исследования чрезвычайно важны для стратификации риска и составления прогноза болезни. Зная мутацию и ее локализацию, можно определить прогноз болезни для каждого конкретного варианта и дать рекомендации по ведению больного, но для этого ключевым моментом является интерпретация данных генетического исследования сначала биоинформатиками для определения патогенности мутации (к сожалению, в нашей стране пока очень мало квалифицированных биоинформатиков), молекулярными биологами для определения функциональных нарушений в белке, вызванных мутацией, и на последнем этапе - кардиологов, которые дадут практические рекомендации по ведению больных и предотвращению осложнений.
18.01.2017 Источник: infox.ru