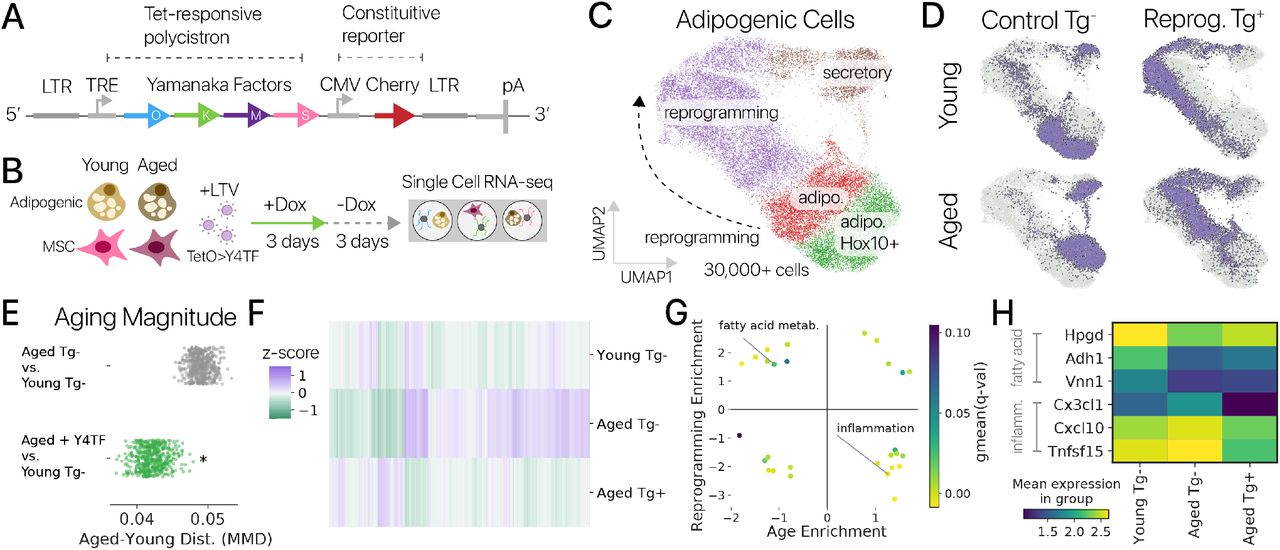
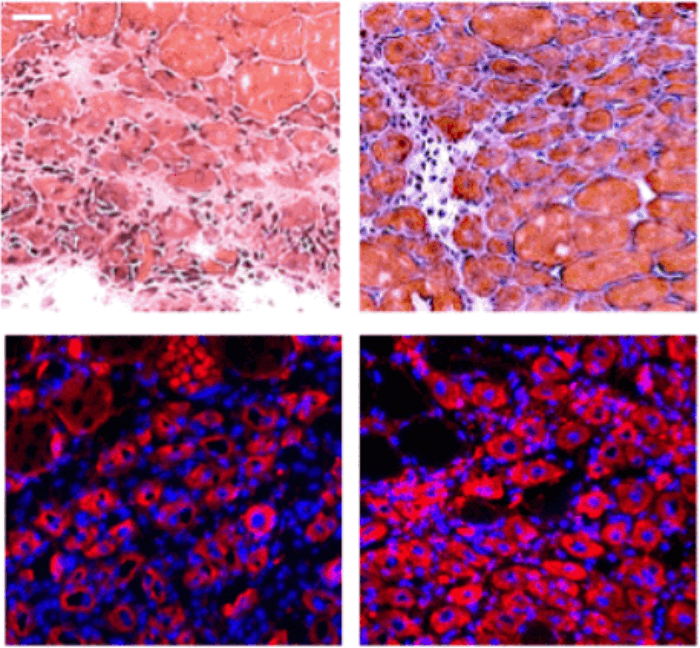
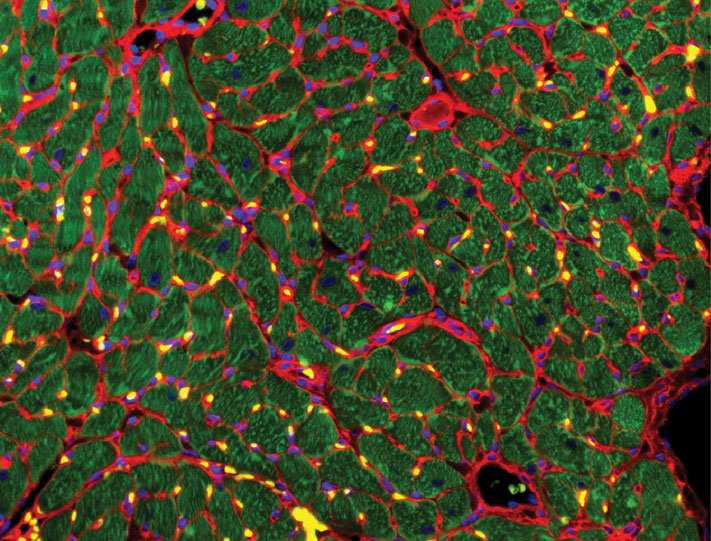
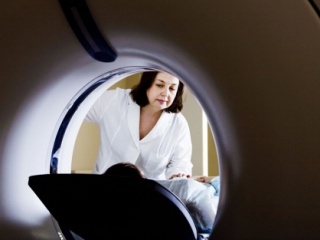
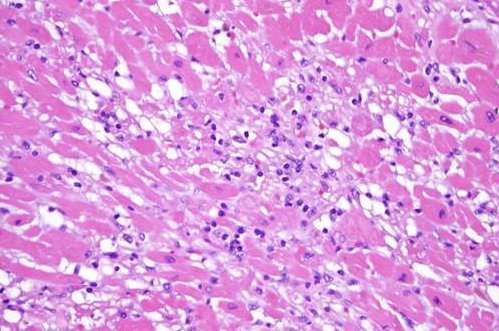
 Ткань мёртвого пациента под микроскопом: видны T-клетки иммунной системы — тёмные синеватые точки, — которые вторглись в мышечные волокна сердца и атакуют их.
Ткань мёртвого пациента под микроскопом: видны T-клетки иммунной системы — тёмные синеватые точки, — которые вторглись в мышечные волокна сердца и атакуют их.
Уотербери (Waterbury), Коннектикут, начало сентября, воскресенье. Пока Чак Пил лежал в отделении неотложной помощи, врачи изо всех сил пытались осмыслить его симптомы. 61-летний Пил, казалось, умирал, а почему, было не очень понятно.
Сознание Пила то возвращалось к нему, то уходило, его кровяное давление резко упало, уровень калия взлетел, а уровень сахара в крови в 10 раз превысил норму. Доктор подозревал сердечный приступ, но неуверенность вынудила его продолжать экстренно исследовать сложившуюся ситуацию по телефону.
Это не был сердечный приступ. Тело Пила терзало само себя — жестокая реакция его иммунной системы, побочный эффект чудотворного, как казалось, лечения рака, которое должно было спасти больному жизнь.
На протяжении семи предшествующих недель доктора Йельского университета сражались с меланомой Пила, используя два препарата, которые в настоящее время входят в число самых многообещающих при лечении рака. Данные лекарства стимулируют иммунную систему атаковать раковую опухоль, причём со свирепостью, свойственной таким мастерам атаки, как вирусы и бактерии.
Применение этих так называемых препаратов иммунотерапии объявлено прорывом в лечении рака. Такая реклама привлекает миллиарды долларов для проведения дальнейших исследований и даёт новую надежду пациентам, у которых нет других вариантов. Но с ростом применения препаратов иммунотерапии становится всё яснее, что они несут с собой серьёзные риски. Корень этих рисков в той самой причине, которая делает препараты эффективными. Стимулированная иммунная система может атаковать здоровые, жизненно важные органы, в особенности кишечник, печень и лёгкие, но, кроме того, почки, надпочечники, гипофиз, поджелудочную железу и, в редких случаях, сердце.
Доктора Йельского университета полагают, что иммунотерапия вызывает новый тип быстро прогрессирующего диабета, таких пациентов у них было по меньшей мере 17, и Пил в их числе. В онкологических клиниках по всему миру и при испытании препаратов выявлено несметное число других побочных эффектов. Исследования говорят о том, что серьёзные осложнения наблюдаются почти в 20 процентах случаев использования определённого препарата и более чем в половине тех случаев, когда какие-то препараты используются в комбинации.
Как показало ещё одно недавнее исследование, у 30 процентов пациентов наблюдались «интересные, редкие или неожиданные побочные эффекты». Четверть этих реакций отнесена к серьёзным, опасным для жизни или требующим госпитализации. Некоторые пациенты умерли, из них пятеро — во время проводившихся в последние месяцы клинических испытаний нового препарата иммунотерапии, разработанного компанией Juno Therapeutics Inc.
Как следствие, говорят онкологи и иммунологи, медицина должна стать более бдительной по отношению к препаратам иммунотерапии, несмотря на их стремительно растущую популярность. И, кроме того, считают они, нужны дополнительные исследования, чтобы выяснить, у кого с наибольшей вероятностью возникают нежелательные побочные эффекты и как их лечить.
«Мы играем с огнём», — сказал доктор Джон Тиммерман (John Timmerman), онколог и исследователь иммунотерапии Калифорнийского университета в Лос-Анджелесе (University of California, Los Angeles), недавно потерявший пациентку из-за побочных эффектов. По словам доктора, препараты иммунотерапии успешно «растворили» её рак, но несколько недель спустя она простудилась и по симптомам её болезнь напоминала грипп. Женщина умерла в отделении реанимации от воспалительного процесса, который доктор Тиммерман описал как «массовый бунт, восстание» её иммунной системы.
«Нам говорили об иммунотерапии, как о подарке Бога, уникальном эликсире, лекарстве от рака, — сказал он. — Нам почти ничего не говорили про сопутствующий вред».
Несмотря на предостережения, врачи, подобные доктору Тиммерману, остаются чрезвычайно благосклонными к препаратам, которые спасают от смерти тех, кому без них не выжить. Логика такая: намного лучше бороться с диабетом, гепатитом или артритом, чем умереть. В своём большинстве побочные эффекты не так уж вредны и поддаются лечению.
Главное препятствие, считают доктора и исследователи, состоит в том, что основные звенья системы онкологической помощи (медсёстры приёмного покоя — онкологи — отделения реанимации) слишком часто попадают в неожиданные ситуации. Это происходит по ряду причин. Во-первых, так как препараты новые, множество вызываемых ими побочных эффектов попросту не успели выявить. Во-вторых, эти эффекты возникают непредсказуемо, иногда спустя месяцы после лечения, и поначалу могут казаться безвредными. Наконец, в настоящее время, чтобы лечить пациентов эффективней, онкологи пробуют применять комбинацию двух или более препаратов иммунотерапии. При этом иногда возрастают риски.
Тем временем препараты иммунотерапии из исследовательских центров попадают в городские онкологические клиники по всей стране, и чем меньше город, тем, весьма вероятно, меньше знают о побочных эффектах местные онкологи.
Что касается жизней, которые будут спасены, и миллиардов долларов, которые будут на это потрачены, — некоторые курсы лечения стоят по прейскуранту 250 000 долларов в год или больше, — то риски новых форм терапии исследованы недостаточно, считает Уильям Мерфи (William Murphy), профессор дерматологии Калифорнийского университета в Дейвисе (University of California, Davis), который следит за субсидиями, выделяемыми местным властям на развитие иммунотерапии.
По словам доктора Мерфи, о рисках, связанных с иммунотерапией, «почти ничего неизвестно». «В первую очередь следует изучать противораковые эффекты. Остальные эффекты, пусть и очень серьёзные, считают ценой, которую стоит платить», — добавил он.
Такие пациенты, как Пил, оказались между двух огней. Их истории демонстрируют щекотливость перекраивания иммунной системы. Оно может стать ключом к лечению рака, если будет сразу и натравливанием, и укрощением.
Реальные перспективы и реальные риски
В июне 2015 года, когда мистер Пил, тощий, в очках, боролся с меланомой, добравшейся до его лёгких, он встретился с йельским онкологом доктором Харриет Клюгер (Harriet Kluger). В прошлом у таких пациентов, как он, шансов поправиться почти не было.
«Мы усадили бы пациента и обратились бы к нему так: «Искренне сожалеем, но у вас остаётся примерно девять месяцев. Приведите свои дела в порядок»», — сказала доктор Клюгер, которая руководит клиническими исследованиями в области иммунотерапии, сфокусированными на лечении кожного и почечного рака.
Теперь она могла вселить в мистера Пила надежду. Судите сами: одно из исследований, проведённых в соавторстве с доктором Клюгер, дало положительные результаты для более чем 40 процентов больных с прогрессирующей меланомой, комбинированно принимавших два главных препарата иммунотерапии — ниволумаб (nivolumab) и ипилимумаб (ipilimumab).
Другое исследование, однако, свидетельствует о том, что ожидаемый лечебный эффект приходит вместе с реальными рисками. Согласно статье 2015 года, опубликованной в The New England Journal of Medicine, использование указанных препаратов несло риск серьёзных, требующих госпитализации или опасных для жизни побочных эффектов в 54 процентах случаев.
«Это, по меньшей мере, много, по меньшей мере», — сказала доктор Клюгер. Но, отметила она, большей частью побочных эффектов можно управлять, используя подавление иммунной системы, например, стероидами.
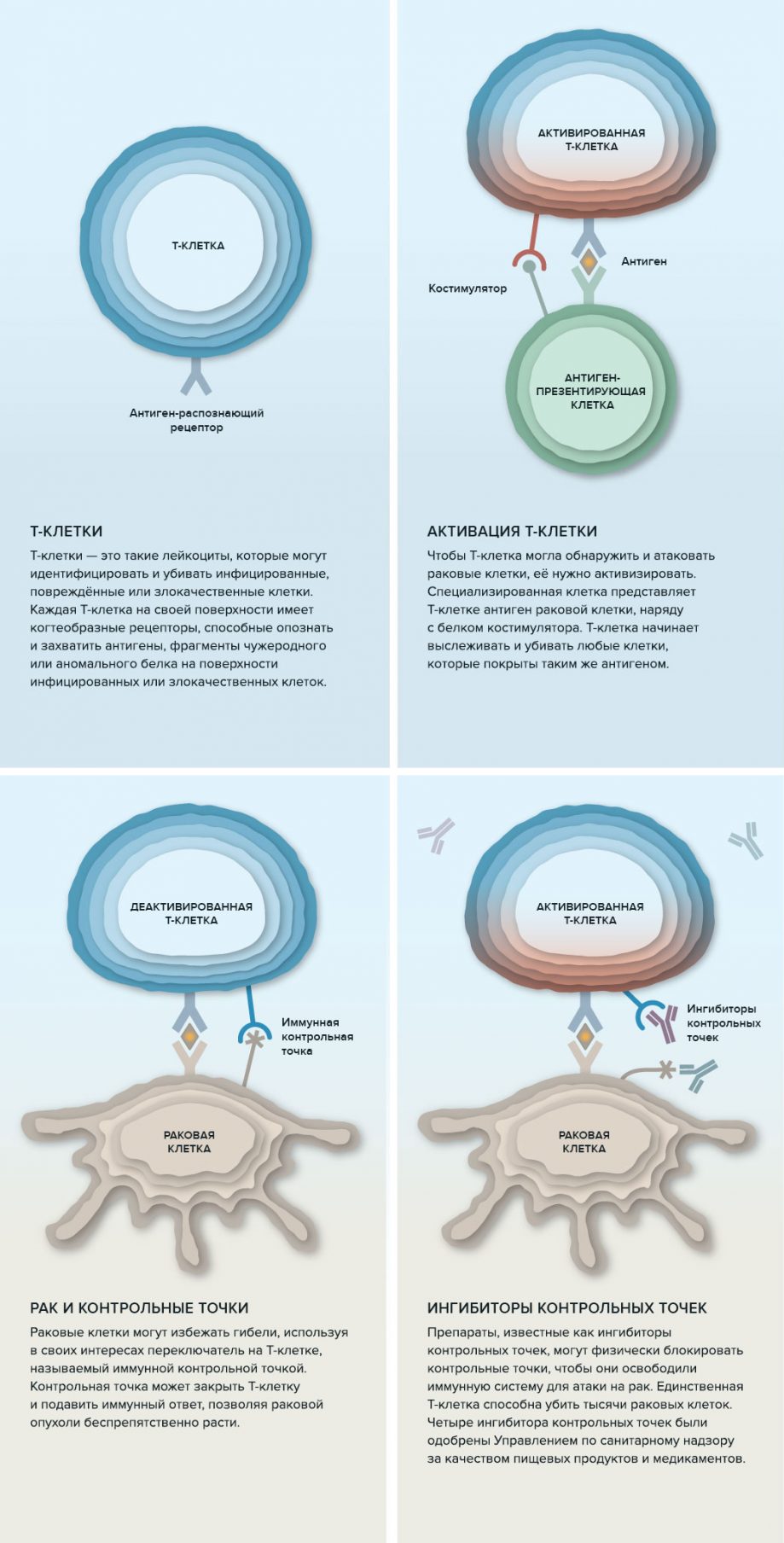
Эффективность препаратов иммунотерапии и их побочные эффекты тесно связаны, так как и тут и там работают одни и те же биологические механизмы.
Рак включает тормоз иммунной системы, посылая её клеткам гнусные сигналы, которые нейтрализуют иммунную защиту. Такой же, в сущности, трюк, но направленный против рака, выполняют препараты иммунотерапии. За это их называют ингибиторами иммунных контрольных точек.
Торможение иммунной системы бывает полезным: оно может остановить мощных защитников тела, чтобы от их атаки случайно не пострадало само тело. Этот исключительно важный для организма механизм выживания рак использует в своих интересах.
Когда препарат иммунотерапии выключает тормоз иммунной системы, иммунные клетки в некоторых случаях могут существенно уменьшить опухоль за считаные дни.
Мистер Пил, инженер-техник, который тестирует работу вертолётных узлов, начал принимать ниволумаб и ипилимумаб 8 июля. Доктор Клюгер сказала ему, что возможны сонливость или тошнота, появление сыпи. 30 августа действительно обильно выступила сыпь: красные волдыри от колен до пояса. 1 сентября, в четверг, доктор Клюгер, осмотрев Пила в своём кабинете, прописала ему стероид.
На следующий день Пил испытал приступы лихорадки, тошноты и, по его словам, «умирал от жажды — хуже, чем в пустыне». Его тошнило от всего. Подруга Пила Джоанн Китинг (Jo-ann Keating) позвонила в офис доктора Клюгер, и дежурный врач прописал таблетки от тошноты. Чуть позже миссис Китинг позвонила ещё раз, чтобы сказать, что лекарство не действует, и врач прописал другие таблетки. В воскресенье, под утро, Пил, не имея возможности передвигаться самостоятельно, вызвал санитарную машину, и его отвезли в отделение неотложной помощи.
В бумажнике Пила лежала информационная карта фармацевтической компании «Бристоль-Майерс Сквибб» (Bristol-Myers Squibb) с длинным списком рисков, которые владелец карты должен иметь в виду. В частности, она информирует Пила о том, что терапия «может вызвать во многих органах вашего тела серьёзные побочные эффекты, способные привести к смерти». Семья Пила, вспоминает миссис Китинг, известила врача из отделения неотложной помощи о лечении, которое проходил Пил.
«Доктор всё говорил, что у Пила была химиотерапия, — рассказывает она. — Я поправила его: „Это называется иммунотерапией“. Он достал телефон и стал искать информацию».
Но даже опытная команда доктора Клюгер, которая в то воскресенье откликнулась на звонки обеспокоенного врача из отделения неотложной помощи, была застигнута врасплох и не сразу определила, как правильно отреагировать на симптомы, проявившиеся у Пила.
«Мы были страшно удивлены. В пятницу он выглядел отлично», — сказала доктор Клюгер. По её мнению, отчасти проблема возникла из-за того, что Пил стал пациентом клиники сравнительно недавно. Так что у неё и её сотрудников не было возможности точно оценить его состояние. «К тому же всё произошло очень быстро. Здоровье пациента резко ухудшилось за считаные часы».
В итоге Пил провёл в больнице 24 дня, и ему становилось всё хуже и хуже. Сначала дала сбой его поджелудочная железа, потом воспалился кишечник и отказали почки. «В довершение всего, он то приходит в сознание, то теряет его, а почему — непонятно», — сказала доктор Клюгер в интервью, которое она дала во время этого кризиса. Она пыталась разобраться в сложившейся ситуации и связалась по электронной почте с другими экспертами со всех концов страны, чтобы узнать, был ли у них когда-нибудь пациент со сходной совокупностью острых иммунных реакций. Оказалось, что не было.
Особо следует отметить сбой поджелудочной железы. Число случаев, когда возникает такая проблема, растёт, и это привело йельского эндокринолога доктора Кевана Херолда (Kevan Herold), крупного специалиста в области аутоиммунных процессов, к выводу, что имеет место новая форма диабета первого типа. Как правило, данная болезнь проявляет себя у детей в возрасте от 6 до 12 лет. Иммунная система постепенно разрушает клетки поджелудочной железы, которые вырабатывают инсулин, необходимый для метаболического превращения сахара в энергию.
И вот картина болезни стала другой: возраст пациентов — 50 лет и больше (в одном случае — 83 года), при этом резко прекращается выработка клетками инсулина. Подобные истории, утверждает доктор Херолд, ему рассказывали коллеги из разных концов страны. «Каждый такой случай необычен, — сказал он. — Как совокупность, это неслыханно».
А вот ещё один йельский случай: пациентка — 65-летняя Коллин Платт (Colleen Platt), агент по продаже недвижимости из Торрингтона (Torrington), Коннектикут. Доктор Клюгер лечила её от почечного рака последней стадии. Миссис Платт выбрала клиническое исследование с использованием двух препаратов иммунотерапии: атезолизумаба (atezolizumab) и второго препарата, название которого доктор Клюгер предпочла сохранить в тайне, так как исследование ещё продолжается.
Через несколько дней после второго курса лечения в ноябре 2014 года миссис Платт стала испытывать головокружение и онемение конечностей. Её рвало водянистой жидкостью. В офисе доктора Клюгер она прошла лабораторное тестирование. Результаты, рассказывает доктор Клюгер, «были настолько аномальными, что мы решили, будто произошла ошибка. Нам показалось, что дело в неисправности лабораторной техники».
Но тестирование было проведено правильно. Как и мистер Пил, миссис Платт вошла в состояние диабетического кетоацитоза, при котором её тело, отчаявшись компенсировать потерю энергии из-за отказа поджелудочной железы, создаёт кислотный поток, способный в течение короткого времени поддерживать функционирование тела, но создающий серьёзную угрозу всем органам. Покинув отделение неотложной помощи, когда туда пришёл священник, чтобы успокоить миссис Платт, доктор Клюгер связалась с фармацевтической компанией и сообщила об экстраординарной реакции на препараты иммунотерапии.
Сейчас, как и мистер Пил, миссис Платт по нескольку раз в день принимает инсулин, и тем не менее уровень сахара в её крови бешено пляшет. С другой стороны, иммунотерапия существенно потеснила её рак. В результате, после консультации с другими врачами и с представителями одной из фармацевтических компаний, доктор Клюгер рекомендовала миссис Платт продолжить начатый курс лечения.
«Её поджелудочную железу вылечить не удаётся, — сказала доктор Клюгер, комментируя диабетические эффекты иммунотерапии, проявившиеся у миссис Платт. — Такова её жизнь».
Мистер Пил, который, как и миссис Платт, разрешил доктору Клюгер и доктору Херолду разбираться с его болезнью, чувствует, что сделка получилась удачной. И в самом деле: в пятницу Пил получил на руки результаты сканирования, проведённого накануне, и узнал, что иммунотерапия избавила его тело от двух очагов рака, а ещё два сделала меньше. «Я могу иметь дело с диабетом, — сказал он, — если я могу бить меланому».
«Природа животного»
Об этих проблемах говорят десятилетия.
В середине 1990-х Мэттью Круммель (Matthew Krummel), молодой аспирант-иммунолог, известный как Макс, работал в лаборатории Университета Калифорнии, Беркли, который позднее стал одним из самых влиятельных центров развития иммунотерапии. Лабораторией руководил доктор Джеймс Аллисон (James Allison). В 1995 году он и Круммель опубликовали результаты фундаментального исследования, согласно которому у мышей можно устранять опухоли, выключая тормоз иммунной системы.
Меньший интерес вызвал побочный эффект проведённого в лаборатории эксперимента: шкурка некоторых мышей, подвергшихся иммунотерапии, поменяла свой цвет с чёрного на белый. В результате атаки иммунной системы на клетки, которые вырабатывают меланин, мех потерял пигментацию. Этот потрясающий эффект не был опасным для жизни мышей, но он показал, насколько серьёзными могут быть последствия поправок, внесённых в работу иммунной системы.
Данное открытие было неординарным, но его затмило другое — то, что обещало излечить рак, вспоминает доктор Круммель. Результаты исследования мышиного меха «были текстом для сноски», добавил он.
Потом, в 2006 году, произошла трагедия TeGenero.
Компания TeGenero Immuno Therapeutics создала препарат, стимулирующий иммунную систему бороться с лейкемией. В лондонской больнице Нортвик Парк (Northwick Park Hospital) было проведено клиническое испытание первой фазы, в ходе которого шесть здоровых добровольцев принимали новый препарат. За считаные часы все участники испытания заработали множественную недостаточность внутренних органов.
Этот разрушительный результат поумерил энтузиазм и заставил увидеть, что работа, которая предшествовала испытанию нового препарата на людях, оказалась недостаточной. Но вскоре энтузиазм бурно возродился. Отчасти потому, что, в конечном счёте, специалисты расценивали возникающие при использовании новых препаратов нежелательные аутоиммунные реакции не только как допустимые побочные эффекты, но и как свидетельство того, что эти препараты работают.
«Это — природа животного, — сказал Мартин Бахманн (Martin Bachmann), профессор-иммунолог Дженнеровского института (Edward Jenner Institute for Vaccine Research), который является филиалом Оксфордского университета. — Я не уверен, что можно избавиться от побочных эффектов, — в действительности, это то, что нужно».
Химиотерапия также имеет побочные эффекты, но доктор Клюгер предпочитает компромисс, который предлагает иммунотерапия, потому что препараты иммунотерапии позволяют устойчиво контролировать рак без длительного курса лечения. Таким образом, она присоединяется к тем, кто хочет ответить на вопросы, в значительной степени оставшиеся без ответа: кому из пациентов грозит опасность, можно ли заблаговременно выявить опасные побочные эффекты и как их устранять?
В июне доктор Клюгер и доктор Херолд подали в Национальный Институт Здоровья заявку на грант, чтобы получить средства для проведения исследования возможности предсказывать, у каких пациентов проявятся опасные побочные эффекты. В основу этого исследования положена гипотеза о существовании у некоторых пациентов биологических особенностей или генетической предрасположенности, которые делают высокой вероятность появления побочных эффектов. Заявка всё ещё рассматривается.
К настоящему времени для ответа на поставленные выше вопросы сделано ничтожно мало. В ряде исследований установлено, что из мышей более чувствительны к аутоиммунным реакциям те, что постарше; другое исследование, в котором также участвовали мыши, обнаружило, что полнота увеличивает риск проявления неблагоприятных эффектов.
«Старые или жирные мыши дохли буквально за считаные часы», — говорит доктор Мерфи, профессор из Дейвиса, по мнению которого исследований на данную тему слишком мало. Ему очень удобно следить за развитием иммунотерапии: в прошлом году он участвовал в работе восьми государственных комитетов, которые рассматривали заявки иммунологов на получение грантов, и, по его словам, только три из 500 заявок связаны с изучением токсичности иммунотерапии.
Отчасти, говорит Мерфи, проблема в том, что фармацевтические компании, которые разрабатывают препараты иммунотерапии, предпочитают иметь дело с лабораториями, которые быстро переходят от одних испытаний к другим. В результате, отмечает доктор Мерфи, испытания на людях продвигаются слишком быстро, а фундаментальные исследования плетутся в хвосте.
В надежде ускорить доступ к препаратам, спасающим жизнь, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов ввело «статус терапии прорыва», который позволяет лекарству быстрее получить одобрение. С 2012 года агентство наделило этим статусом примерно 110 лекарств, и почти четверть из них — препараты иммунотерапии.
«Когда люди говорят о „полётах на Луну“, они имеют в виду лечение рака, но нужно видеть картину в целом», — сказал доктор Мерфи.
Прилагая огромные усилия к лечению рака, онкологи — как исследователи, так и лечащие врачи — стараются больше внимания уделять побочным эффектам. Доктор Тиммерман из Калифорнийского университета в Лос-Анджелесе жалеет, что за довольно скромными симптомами, напоминающими грипп, не разглядел смертельную опасность, подкравшуюся к его пациентке, и она пережила рак только для того, чтобы умереть в отделении неотложной помощи.
«Если б мы только знали, что сила, которую мы выпустили на свободу, способна нанести фатальный ущерб её организму, мы могли бы спасти её», — сказал доктор.
«Вы должны управлять этой силой час за часом, — добавил он. — Минута за минутой».
Автор — Мэтт Рихтел (Matt Richtel), 3 декабря 2016 года.
Перевод — Александр Горлов.