Исследователи из университета Райса, работающие под руководством доктора Джеффри Табора (Jeffrey Tabor), создали генетически модифицированные кишечные бактерии, способные реагировать на развитие колита – воспаления кишечника – у мышей. Результаты этой работы указывают новое исследовательское направление, посвященное изучению взаимодействия кишечных бактерий и человека на молекулярном уровне, конечным результатом которого может стать создание пероральных бактериальных препаратов для мониторинга состояния кишечника.
Как говорит доктор Табор, кишечник является домом для миллиардов микроорганизмов, оказывающих влияние на состояние здоровья и течение заболеваний. Однако он представляет собой темное и труднодоступное место, детальное изучение протекающих в котором процессов возможно с помощью очень ограниченного набора технологий. С другой стороны, в ходе эволюции бактерии приобрели десятки тысяч сенсоров, многие из которых реагируют на различные вещества в кишечном тракте. Поэтому генетически модифицированные бактерии-сенсоры обладают огромным потенциалом для изучения протекающих в кишечнике процессов и диагностики заболеваний.
Специалисты по синтетической биологии специализируются на программировании одноклеточных организмов, таких как бактерии, с помощью подходов, схожих с подходами, позволяющими инженерам программировать роботов. В частности, Табор и его коллеги работают над созданием бактериальных сенсоров, позволяющих регистрировать сигналы заболеваний кишечника. Подобно инженерам-электрикам, создающим электрические цепи из проводов и электронных деталей, они используют генетические цепи для программирования одноклеточных организмов, приобретающих в результате способность к сложной обработке информации.
Результаты более ранних исследований авторов свидетельствуют о том, что изменения микробиома кишечника, генетическая предрасположенность и различные факторы внешней среды могут играть ключевые роли в развитии воспалительной болезни кишечника – достаточно распространенного сборного состояния, включающего болезнь Крона и неспецифический язвенный колит.
На основании результатов ряда более ранних работ исследователи предположили, что развитие колита сопровождается повышением содержания тиосульфата в содержимом кишечника. Изучение этой взаимосвязи на сегодняшний день затруднено из-за отсутствия инструментов для достоверной оценки уровня тиосульфата в условиях живого организма. Первой целью запущенного в 2015 году проекта было создание такого инструмента.
Взятая за основу идея заключалась в использовании сенсорных бактерий, а именно генетически модифицированной кишечной палочки (Escherichia coli) для регистрации тиосульфата и родственных ему серосодержащих соединений, которые также могут быть биомаркерами колита. Исследователи имели в своем распоряжении хорошо отработанные методы генетического программирования, наделяющие кишечную палочку способностью продуцировать зеленый флуоресцирующий белок в ответ на специфичные стимулы, однако они не знали, какие гены обеспечивают возможность регистрации тиосульфата и других серосодержащих соединений.
С помощью специальной компьютерной программы такие гены удалось найти в геноме обитающих в морских отложениях бактерий шеванелл (Shewanella). Авторы считают, что шеванеллы используют сенсоры серосодержащих соединений для активации специфичных к ним ферментов.
Около года у них ушло на создание генетически модифицированного штамма кишечной палочки, экспрессирующей гены таких сенсоров, валидацию функционирования этих генов их оптимизацию, обеспечивающую специфичную реакцию на потенциальные биомаркеры, проявляющуюся экспрессией зеленого флуоресцирующего белка. Еще год потребовался для подтверждения функциональности данной системы и ее способности выявлять воспаление кишечника у мышей.
В рамках экспериментов животные с колитом, а также здоровые мыши групп контроля получали перорально по две капли раствора, содержащего примерно миллиард сенсорных бактерий. Через шесть часов исследователи оценивали активность сенсорных бактерий в фекалиях по яркости свечения зеленого флуоресцирующего белка. Это свечение не видно невооруженным глазом, но легко регистрируется с помощью стандартного лабораторного прибора, известного как проточный цитофлуориметр.
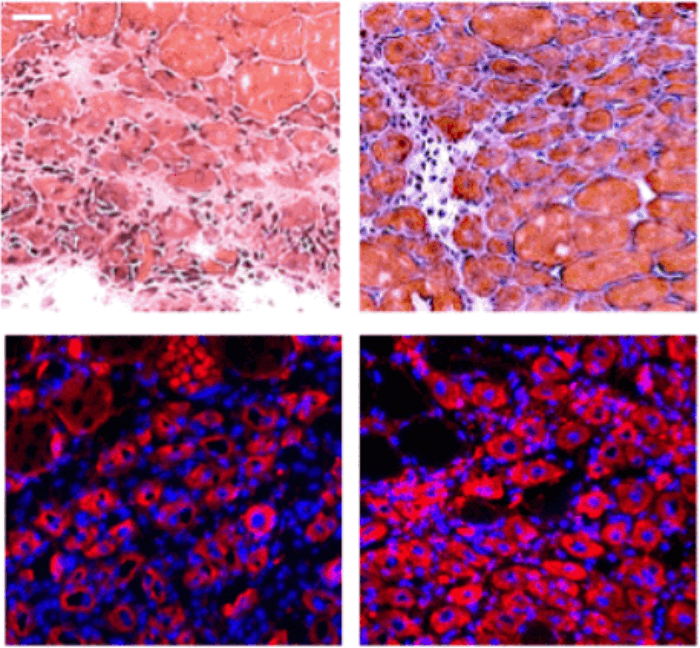
Наблюдения показали, что бактериальный сенсор не активировался в кишечнике здоровых животных, но активировался в кишечнике мышей с воспалением кишечника, при этом яркость флуоресценции была пропорциональная степени воспаления.
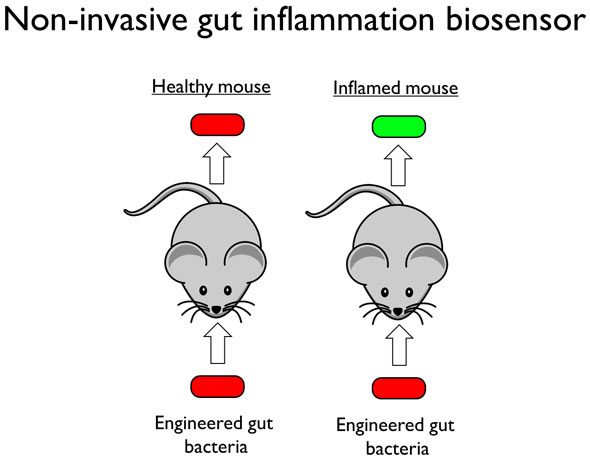
По словам доктора Табора, полученные данные свидетельствуют о том, что несущие генно-инженерные сенсоры бактерии могут использоваться для неинвазивного выявления определенных метаболитов в кишечнике, что предоставит новые возможности в изучении протекающих в нем процессов.
Очевидно, что разработка подходов, пригодных для клинического применения, займет еще несколько лет и на сегодняшний день неясно, является ли тиосульфат биомаркером колита у человека. Однако предложенную авторами технологию можно адаптировать к выявлению других соединений, а зеленый флуоресцирующих протеин можно заменить ферментом, обеспечивающим появление специфичной окраски фекалий. Во многих случаях подобные тесты смогут заменить посещение врача и дорогостоящую инвазивную процедуру колоноскопии.
Статья Kristina N-M Daeffler et al. Engineering bacterial thiosulfate and tetrathionate sensors for detecting gut inflammation опубликована в журнале Molecular Systems Biology.
12.04.2017 Источник: Евгения Рябцева, Портал «Вечная молодость» http://vechnayamolodost.ru по материалам Rice University: Synthetic biologists engineer inflammation-sensing gut bacteria.