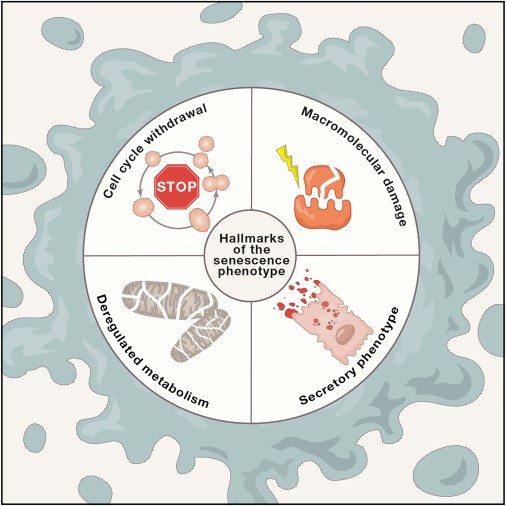
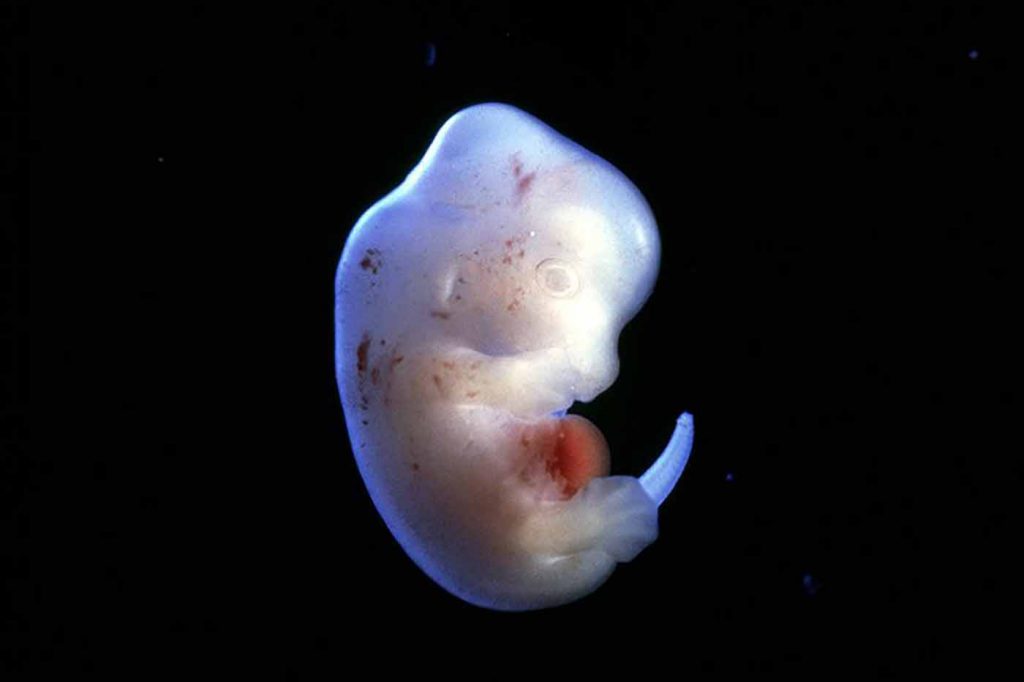
Недавно в журнале Nature была опубликована статья, рассказывающая об успешном исправлении мутации в ДНК человеческого зародыша при помощи геномного редактора CRISPR/Cas9. Возможность устранения ошибок в геноме ведет к абсолютно новой ситуации, которая разворачивается на наших глазах. По сути, эта технология может положить конец биологической эволюции, которая представляет собой генетически наследуемое изменение организма в процессе адаптации к окружающей среде.
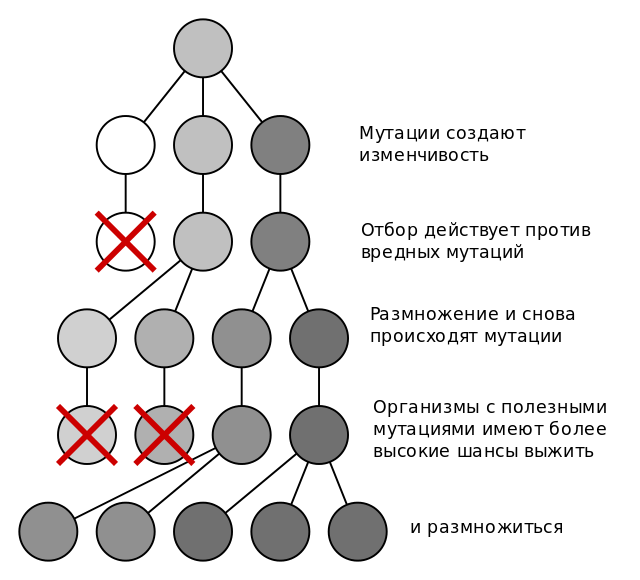
Эволюционный процесс основан на двух важных факторах: естественном отборе под влиянием среды (направленные изменения) и фиксации случайных мутаций (ненаправленные изменения), которые ведут к изменению существующих и возникновению новых признаков. Если выброшенные эволюционным мутационным лототроном "шары" случайных мутаций оказываются вдруг выгодны для данного организма и вида, они поддерживаются естественным отбором.
 Пример эволюции вьюрков в изоляции на Галапагосских островах
Пример эволюции вьюрков в изоляции на Галапагосских островах
Эти организмы приобретают преимущество и размножаются, то есть увеличивается их приспособленность, основными компонентами которой являются выживаемость и фертильность (плодовитость). Кроме этого, есть еще случайный процесс, своего рода генетическая лотерея, называемая генетическим дрейфом, в ходе которого могут фиксироваться даже вредные мутации и теряться полезные. Он наиболее выражен в малочисленных популяциях, где случай может играть существенную роль.
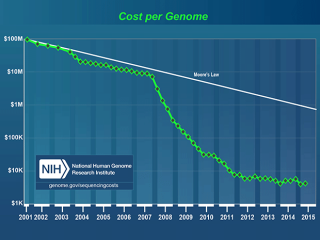
В начале ХХI века генетика продвинулась так далеко, что человечество получило возможность контролировать не только факторы среды, но и исправлять мутации.
Поясняет профессор Геттингенского университета (Германия) и Техасского университета А&М (США), ведущий научный сотрудник Института общей генетики имени Н. И. Вавилова РАН и pyководитeль Научно-образовательного центра геномных исследований Сибирского федерального университета (Красноярск) Константин Крутовский:
"Взять, к примеру, такую болезнь, как фенилкетонурия, — наследственное заболевание, связанное с нарушением метаболизма аминокислот, которое приводит к накоплению фенилаланина и его токсических продуктов.
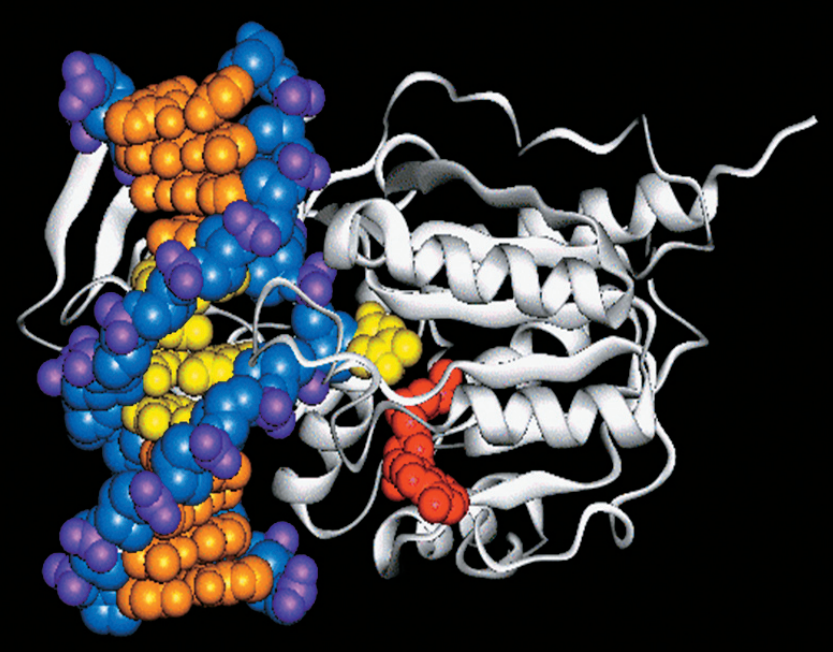
Известно, что эта болезнь приводит к тяжелому поражению центральной нервной системы и нарушениям умственного развития. Так вот, фенилкетонурия — это одно из немногих наследственных заболеваний, причина которого в мутации всего одного гена, а иногда и единственного нуклеотида в нем (ген РАН — Phenylalanine hydroxylase).
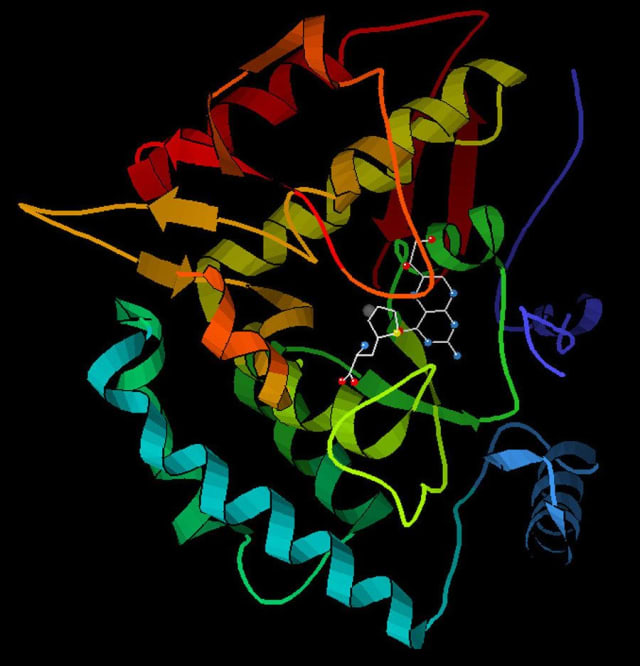 Фенилаланингидроксилаза (PAH)
Фенилаланингидроксилаза (PAH)
Раньше эта мутация являлась летальной. Приспособленность особей, родившихся с фенилкетонурией, была равна нулю, они обычно погибали в двух-, трехлетнем возрасте. Но поскольку сейчас причина этой болезни известна, то она легко корректируется с помощью специальной диеты, которая ограничивает поступление фенилаланина. Это — корректировка фактора среды. Но развитие генетики пошло еще дальше! Теперь ученые могут заменить мутантный аллель (вариант гена) на немутантный в гене РАН на самой ранней стадии развития эмбриона".
Фктически это означает, что у человечества появилась возможность контролировать оба фактора биологической
Фактически это означает, что у человечества появилась возможность контролировать оба фактора биологической эволюции, что и означает ее конец.
эволюции, что
Дальше можно фантазировать. Как человечество распорядится новыми возможностями? Конечно, для матери всегда будет важно иметь здорового ребенка. С этой точки зрения корректировка генома обязательно будет введена в прейскурант центров репродукции, а зачатие сведется к точечной подсадке «идеального» эмбриона в матку.
Интересно, что некое подобие выбора эмбрионов осуществляется уже сейчас, в практике экстракорпорального оплодотворения. Эмбриолог всегда имеет несколько зародышей на стадии бластоцисты, чтобы выбрать из них один и подсадить его в матку.
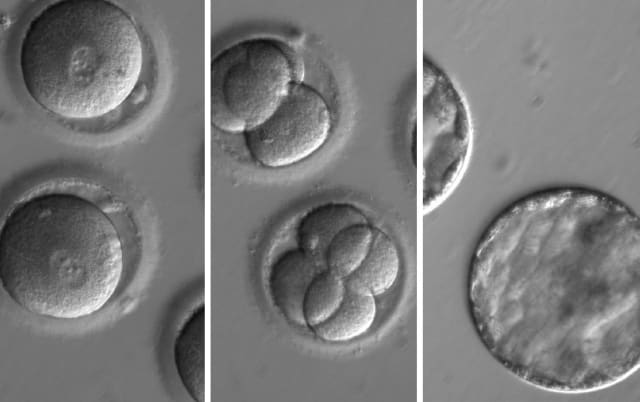 Превращение в бластоцисту
Превращение в бластоцисту
По какому же принципу происходит отбор? Конечно, врачи знают, какой формы должен быть зародыш, чтобы он хорошо прижился. Однако никто не представляет себе, какими по форме зародышами были Роберт Шуман, Михаил Врубель, Федор Достоевский, известнейший ученый современности Стивен Хокинг… Вдруг, исключив «некрасивые» бластоцисты, мы лишимся гениев в целой популяции?
Комментирует Константин Крутовский:
"В случае заболевания Стивена Хокинга все довольно просто. Думаю, что через несколько лет мы научимся лечить боковой амиотрофический склероз (БАС, ALS), известный также как болезнь Лу Герига.
Как и многие нейродегенеративные заболевания, БАС определяется по накоплению аномальных белков в мозге. На 10-20% БАС генетически обусловлен и связан с мутациями в некоторых генах. А если речь идет об одном или нескольких генах — значит, «спасение» уже близко. Насколько я знаю, никаких корреляций между интеллектуальными способностями и болезнью Лу Герига нет. Но если они все-таки есть, хотелось бы спросить у самого Хокинга: готов ли он был бы пожертвовать своей гениальностью, чтобы ходить, играть в мяч, плавать в океане, — жить как все обычные люди?"
 Стивен Хокинг - английский физик-теоретик и популяризатор науки
Стивен Хокинг - английский физик-теоретик и популяризатор науки
Есть еще одна опасность, которую таит в себе развитие геномного редактирования. Если мы будем стремиться создать по определенным алгоритмам "идеальный", долго живущий, абсолютно здоровый геном, это приведет к уменьшению генетического разнообразия. А ведь именно оно является материалом естественной эволюции, страховкой человечества от неизвестных новых (или хорошо "забытых") форм злокачественных бактерий и вирусов, которые еще не полностью исчезли или могут быть занесены из космоса.
14.08.2017 Источник: ria.ru