Дифференцировка стволовых клеток, то есть их превращение в тот или иной клеточный тип, — это сложный многоступенчатый процесс. По пути в конечное состояние клетка проходит ряд промежуточных стадий. Существует два подхода к дифференцировке клеток in vitro. Можно последовательно воспроизводить процессы, происходящие в зародыше при развитии, и постепенно вести клетку в требуемом направлении. А можно сразу экспрессировать в клетке белки, характерные для конечного состояния. Будут ли в этом случае клетки проходить все промежуточные состояния или какие-то пропустят? Или же они вообще пойдут другим путем?
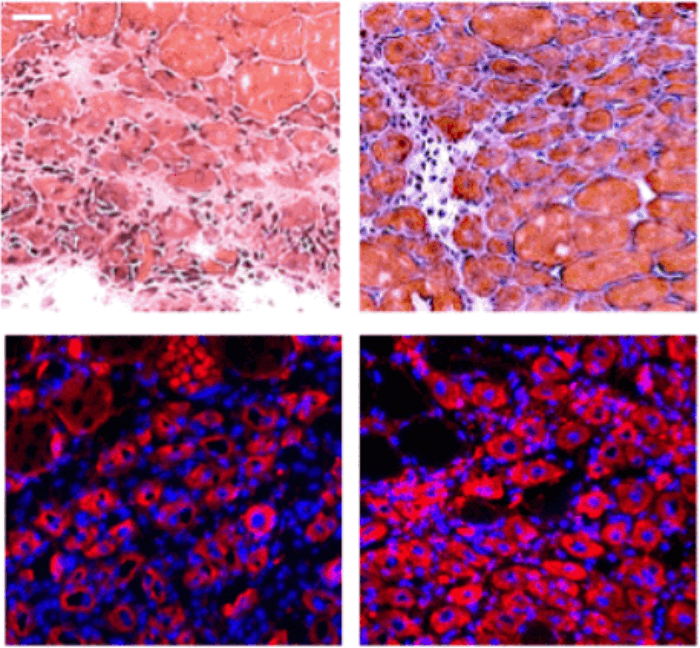
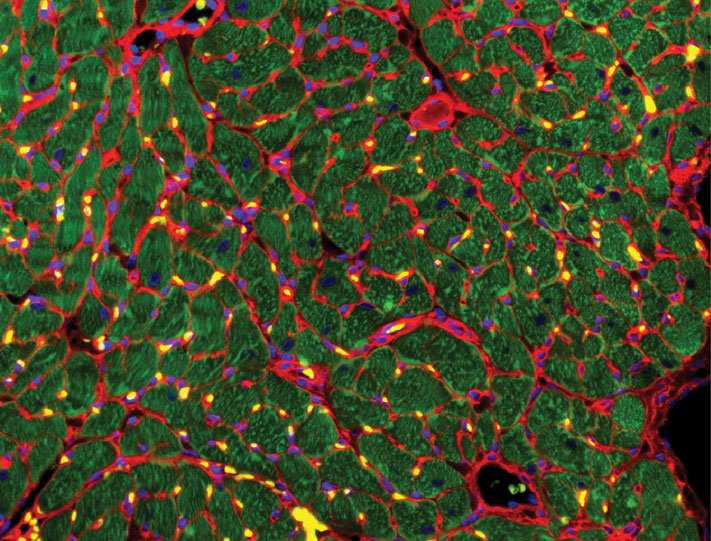
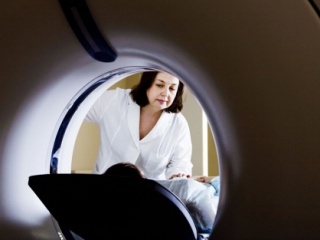
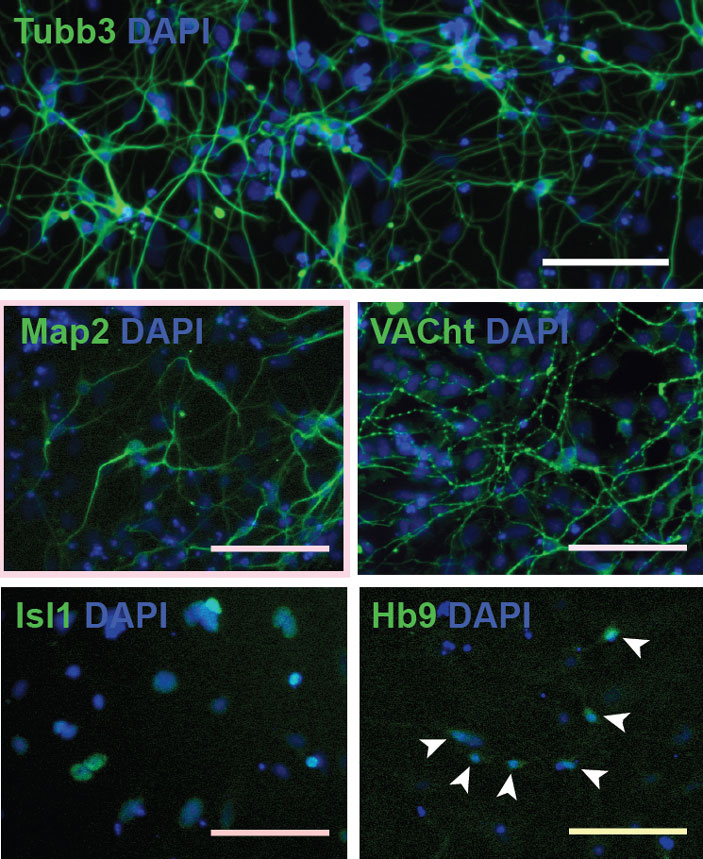 Рис. 1. Моторные (двигательные) нейроны, полученные из стволовых клеток. Голубой — DAPI, ядра клеток. Зеленый — белки, подтверждающие, что эти нейроны функциональны: Tubb3 — тубулин, белок микротрубочек в аксонах; Map2 — белок, связанный с микротрубочками; VACht — белок, транспортирующий вакуоли с нейромедиатором ацетилхолином. Изображение из обсуждаемой статьи в eLife
Рис. 1. Моторные (двигательные) нейроны, полученные из стволовых клеток. Голубой — DAPI, ядра клеток. Зеленый — белки, подтверждающие, что эти нейроны функциональны: Tubb3 — тубулин, белок микротрубочек в аксонах; Map2 — белок, связанный с микротрубочками; VACht — белок, транспортирующий вакуоли с нейромедиатором ацетилхолином. Изображение из обсуждаемой статьи в eLife
Развитие зародыша от зиготы до полноценного организма можно представить в виде дороги со множеством развилок. По мере того как клетки делятся, каждая из них выбирает путь, по которому она будет двигаться дальше, то есть приобретает некоторые характерные свойства (форму, внутреннее строение и экспрессию конкретных генов). В результате множества таких последовательных «решений» клетка достигает конечного состояния — одного из клеточных типов взрослого организма со всем набором его характерных признаков. Весь этот путь клетки в целом называют дифференцировкой, а итог — дифференцированным состоянием.
В 1954 году английский биолог Конрад Уоддингтон предложил модель эпигенетического ландшафта, которая, в частности, применима и к дифференцировке стволовых клеток. Этот ландшафт выглядит как горка с параллельными разветвляющимися колеями (креодами), а клетка представляется шариком, скатывающимся по этой горке (рис. 2.). Согласно этой модели, судьба клетки определяется раз и навсегда, и изменить ее уже не получится. Чтобы клетка оказалась вместо одного органа в другом, ей нужно перескочить в соседнюю колею, что в данной модели энергетически невыгодно.
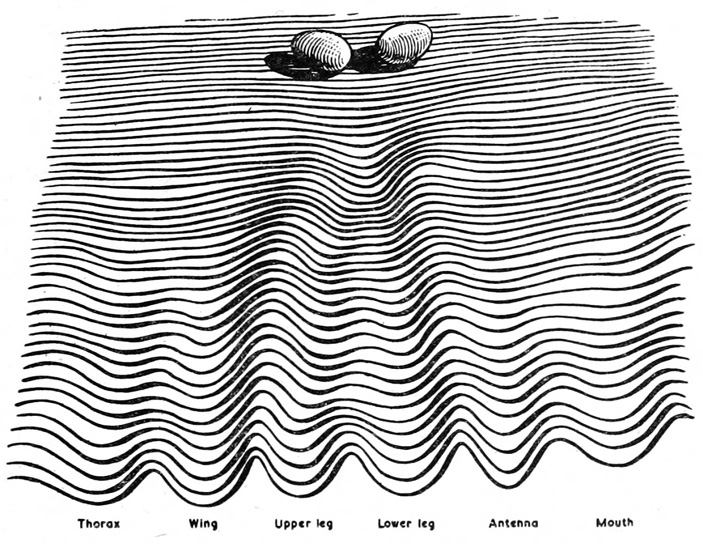 Рис. 2. Эпигенетический ландшафт Уоддингтона. Под каждой колеей указано итоговое предназначение клетки: грудь, крыло, верхняя нога, нижняя нога, антенна, рот (речь идет о развитии дрозофилы). Изображение из книги: C. H. Waddington. «Principles of embryology». NY, 1956.
Рис. 2. Эпигенетический ландшафт Уоддингтона. Под каждой колеей указано итоговое предназначение клетки: грудь, крыло, верхняя нога, нижняя нога, антенна, рот (речь идет о развитии дрозофилы). Изображение из книги: C. H. Waddington. «Principles of embryology». NY, 1956.
Идеи Уоддингтона остаются актуальными до сих пор, однако эксперименты со стволовыми клетками подсказывают нам новые правила обращения с этим ландшафтом. Так, в 2006 году японским ученым Такахаси и Яманаке удалось «забросить камень обратно на гору» — вернуть клетки мыши из терминально-дифференцированного состояния на уровень эмбриональных стволовых клеток зародыша, из которых можно получить любой клеточный тип (см. K. Takahashi, S. Yamanaka, 2006. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors). Для этого в зрелые фибробласты мыши вводили 4 ключевых транскрипционных фактора, обеспечивающих стволовое состояние. Этот процесс назвали репрограммированием клеток. Однако сам Яманака отметил невысокую эффективность этого процесса: в первых экспериментах удавалось репрограммировать лишь 0,05% клеток.
Потом эти цифры выросли, в некоторых случаях даже до 10%, но большинство клеток всё равно не поддавалось методике (см. S. Yamanaka, 2009. Elite and stochastic models for induced pluripotent stem cell generation). Яманака предпринял попытку объяснить это через ландшафт Уоддингтона (рис. 3). Предположим, что мы пытаемся забросить шарик обратно на гору. На его пути может возникнуть несколько препятствий: он может не долететь до верха и скатиться вниз окончательно (в данном случае это означает апоптоз, то есть намеренную гибель клетки, стрелка 4), может докатиться до верха и не удержаться там (тогда клетка будет дифференцироваться снова в случайном направлении, стрелка 2) или может полететь в неправильном направлении и перескочить в соседнюю колею (дифференцироваться в другой тип, стрелка 3). И только в тех редких случаях, когда шарик долетает до верха и удерживается там, клетка репрограммируется и становится стволовой (стрелка 1).
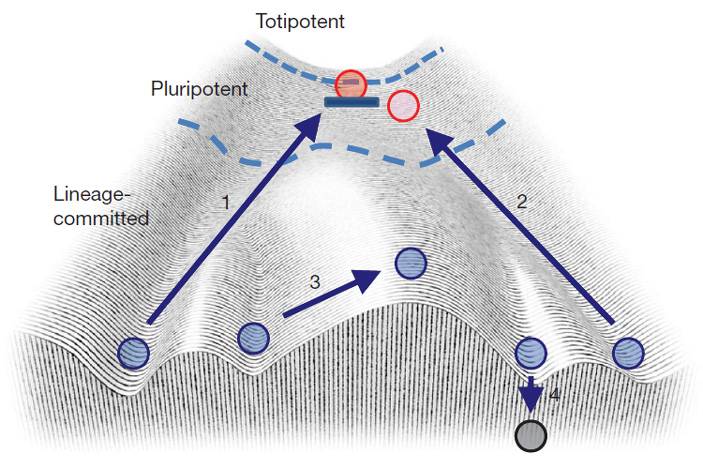
 Рис. 3. Применение ландшафта Уоддингтона к репрограммированию клеток. 1 — полный возврат к эмбриональному состоянию. 2 — неудавшееся репрограммирование. 3 — переход в другой тип клеток. 4 — клеточная гибель. Изображение из статьи: S. Yamanaka, 2009. Elite and stochastic models for induced pluripotent stem cell generation
Рис. 3. Применение ландшафта Уоддингтона к репрограммированию клеток. 1 — полный возврат к эмбриональному состоянию. 2 — неудавшееся репрограммирование. 3 — переход в другой тип клеток. 4 — клеточная гибель. Изображение из статьи: S. Yamanaka, 2009. Elite and stochastic models for induced pluripotent stem cell generation
Но на этом приключения шарика на горке не заканчиваются. До недавнего времени были известны всего две основные методики работы со стволовыми клетками: дифференцировка и репрограммирование. Протоколы дифференцировки состояли из последовательного действия на клетки веществами, «направляющими» их в ту или иную сторону. Набор этих веществ определяли экспериментально, основываясь на реальных процессах развития. Если для дифференцировки клеток нервной системы на некоторой стадии в зародыше мыши нужна ретиноевая кислота, то и в лаборатории можно добавить ее в среду культивирования для получения нейронов. Теперь представим себе, что мы хотим получить, например, культуру нейронов человека. Можно взять его клетки кожи, репрограммировать до эмбриональных стволовых клеток, а затем дифференцировать в нейроны. Это оказывается долго и неэффективно, поэтому давно идет поиск более короткого пути.
Коротких путей обнаружилось два — прямая дифференцировка и трансдифференцировка. В ходе прямой дифференцировки предлагается получить нейроны из эмбриональных стволовых клеток без промежуточных стадий. Трансдифференцировка же предполагает получение нейронов напрямую из клеток кожи. Отметим сразу, что клеточные типы здесь даны как примеры, реально они могут быть практически любыми. Эти короткие пути осуществляются одним способом: в культуре исходных клеток (стволовых или дифференцированных) запускается экспрессия транскрипционных факторов, характерных для нужного клеточного типа (в данном случае, нейронов). Эффективность этих методов пока остается невысокой, однако оба они работают. Поэтому возникает множество вопросов: насколько функциональны полученные таким образом клетки? Какие механизмы лежат в основе ускоренной дифференцировки? Что при этом происходит с промежуточными стадиями, исчезают ли они полностью или частично сохраняются? Этими вопросами и задались авторы обсуждаемой статьи (рис. 4).
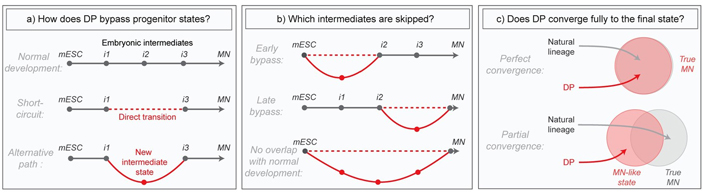 Рис. 4. Исследовательские вопросы авторов обсуждаемой статьи. а) Как в случае прямой дифференцировки обходятся промежуточные стадии? Возможные варианты: все стадии присутствуют, некоторые стадии пропущены, появляются альтернативные стадии. b) Какие из промежуточных стадий исчезают? Возможные варианты: самые ранние, самые поздние, весь путь отличается от классического. с) Получаются ли в результате прямой дифференцировки полноценные функциональные клетки? Возможные варианты: полное или частичное достижение эффекта. Изображение из обсуждаемой статьи в eLife
Рис. 4. Исследовательские вопросы авторов обсуждаемой статьи. а) Как в случае прямой дифференцировки обходятся промежуточные стадии? Возможные варианты: все стадии присутствуют, некоторые стадии пропущены, появляются альтернативные стадии. b) Какие из промежуточных стадий исчезают? Возможные варианты: самые ранние, самые поздние, весь путь отличается от классического. с) Получаются ли в результате прямой дифференцировки полноценные функциональные клетки? Возможные варианты: полное или частичное достижение эффекта. Изображение из обсуждаемой статьи в eLife
Авторы работали с эмбриональными стволовыми клетками мыши. Они запустили параллельно стандартный протокол последовательной дифференцировки и прямую дифференцировку в моторные нейроны спинного мозга. Чтобы отследить, на каких стадиях находятся клетки, они анализировали РНК в отдельных клетках на ранних (4–5 день) и поздних (11–12 день) стадиях дифференцировки. Затем исключали клетки, от которых получено слишком мало РНК, и те, у которых обнаруживали повышенную экспрессию митохондриальных генов, связанных со стрессом: эти клетки, возможно, развивались аномально. В оставшихся клетках вычисляли гены, экспрессия которых статистически значимо менялась в ходе дифференцировки.
Это позволило определить основные стадии, через которые проходили клетки. При стандартном протоколе дифференцировки путь получился следующим: эмбриональные стволовые клетки — общие нейральные предшественники — клетки заднего отдела нервной системы — клетки брюшной стороны заднего отдела — предшественники моторных нейронов — ранние моторные нейроны — поздние (зрелые) моторные нейроны. При этом в культуре можно было обнаружить несколько стадий одновременно, так как клетки дифференцируются асинхронно. Ученые обнаружили, что при использовании стандартного протокола до поздних стадий доходило меньше клеток, чем при прямой дифференцировке, а также больше клеток отклонялось от намеченного пути и превращалось в другие типы. В то же время при прямой дифференцировке не удалось обнаружить двух стадий: клетки не приобретали постепенно свойств заднего и брюшного отделов нервной системы (рис. 5). При этом начальные и конечные стадии в обоих протоколах оказались очень похожими. Итогом стали полноценные и функциональные моторные нейроны.
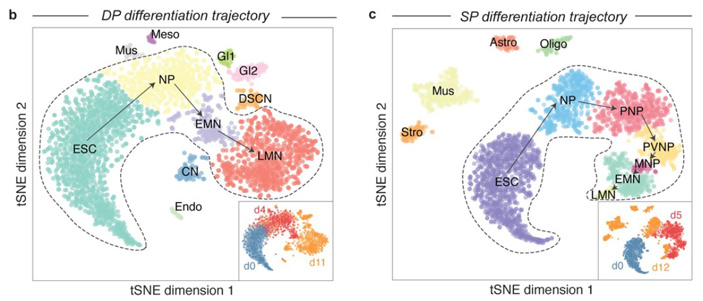 Рис. 5. Последовательные стадии, которые проходят клетки при прямой (b) и постепенной (с) дифференцировке. По осям отложены статистические показатели, отражающие экспрессию характерных для разных стадий групп генов. Клетки с близкими значениями этих показателей считали находящимися на одной стадии. Обозначения стадий: ESC — эмбриональные стволовые клетки, NP — общие нейральные предшественники, PNP — клетки заднего отдела нервной системы, VNP — клетки брюшной стороны заднего отдела, MNP — предшественники моторных нейронов, EMN — ранние моторные нейроны, LMN — поздние (зрелые) моторные нейроны. Изображение из обсуждаемой статьи в eLife
Рис. 5. Последовательные стадии, которые проходят клетки при прямой (b) и постепенной (с) дифференцировке. По осям отложены статистические показатели, отражающие экспрессию характерных для разных стадий групп генов. Клетки с близкими значениями этих показателей считали находящимися на одной стадии. Обозначения стадий: ESC — эмбриональные стволовые клетки, NP — общие нейральные предшественники, PNP — клетки заднего отдела нервной системы, VNP — клетки брюшной стороны заднего отдела, MNP — предшественники моторных нейронов, EMN — ранние моторные нейроны, LMN — поздние (зрелые) моторные нейроны. Изображение из обсуждаемой статьи в eLife
Это отличие прямой дифференцировки от стандартной наглядно показывает нам разницу между развитием клетки в эмбрионе и в культуре. В целостной системе, такой как зародыш, на ранних этапах возникает разметка плана строения, и только после этого начинается окончательная дифференцировка. Вероятно, это необходимо для адекватного взаимодействия между тканями и разными типами клеток в эмбрионе. В то же время эти стадии оказываются не критичными для последующего формирования функционального нейрона, если идет речь о культуре, где клетки не взаимодействуют с окружением. При прямой дифференцировке клетки проходили стадию, нехарактерную для стандартного протокола: в них включались гены переднего мозга. Впрочем, к поздним стадиям их экспрессия исчезала, и конечные стадии дифференцировки в обоих протоколах оказались очень похожими.
Технология прямой дифференцировки вызывает много вопросов и споров. Несмотря на ее эффективность, прежде чем использовать ее на практике, необходимо убедиться в том, что «нестандартные» пути развития клеток не привносят в них никаких побочных свойств. Авторы обсуждаемой статьи полагают, что стадия терминально-дифференцированной клетки относится к числу так называемых «бассейнов притяжения» (см. Basin of attraction), то есть устойчивых состояний, к которым стремятся все незначительно отличающиеся состояния и которые устойчивы к умеренным колебаниям окружающей среды. Это означает, что если в результате дифференцировки каким-либо образом будет достигнута экспрессия ключевых транскрипционных факторов, то клетка так или иначе придет к конечному состоянию. И вероятность того, что она в последний момент пойдет по другому пути, крайне мала. Если это действительно так, то можно ожидать, что короткие пути дифференцировки вскоре вытеснят длинные и традиционные, увеличив эффективность процесса и приблизив нас к использованию этих технологий в медицине.
Подробнее по теме:
Регенеративная медицина, клеточная терапия
Терапия стволовыми клетками эффективно и безопасно борется со старением
Источники: elementy.ru; James Alexander Briggs, Victor C. Li, Seungkyu Lee, Clifford J. Woolf, Allon Klein, Marc W. Kirschner. Mouse embryonic stem cells can differentiate via multiple paths to the same state // eLife. 2017. V. 6. P. e26945. Doi: 10.7554/eLife.26945. Автор: Полина Лосева