Гость программы - Михаил Гельфанд, биоинформатик, руководитель магистерской программы «Биотехнологии» Сколтеха; заместитель директора Института проблем передачи информации РАН
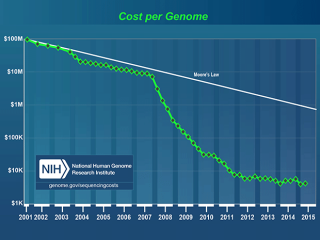
Сергей Медведев: Когда я был ребенком и молодым человеком, я помню, как газеты постоянно трубили: вот-вот что-то будет, когда расшифруют геном человека, когда все эти кубики и кирпичики станут понятны… И вот геном человека расшифрован – что дальше? Появляется наука под названием "биоинформатика". Что это такое? Является ли расшифрованный геном человека неким конструктором, лего, из которого создана человеческая жизнь? У нас в гостях Михаил Гельфанд, биоинформатик, руководитель магистерской программы "Биотехнология" Сколтеха, заместитель директора Института проблем передачи информации РАН.
Михаил Гельфанд: Я еще профессор факультета компьютерных наук Высшей школы экономики и факультета биоинженерии, биоинформатики МГУ.
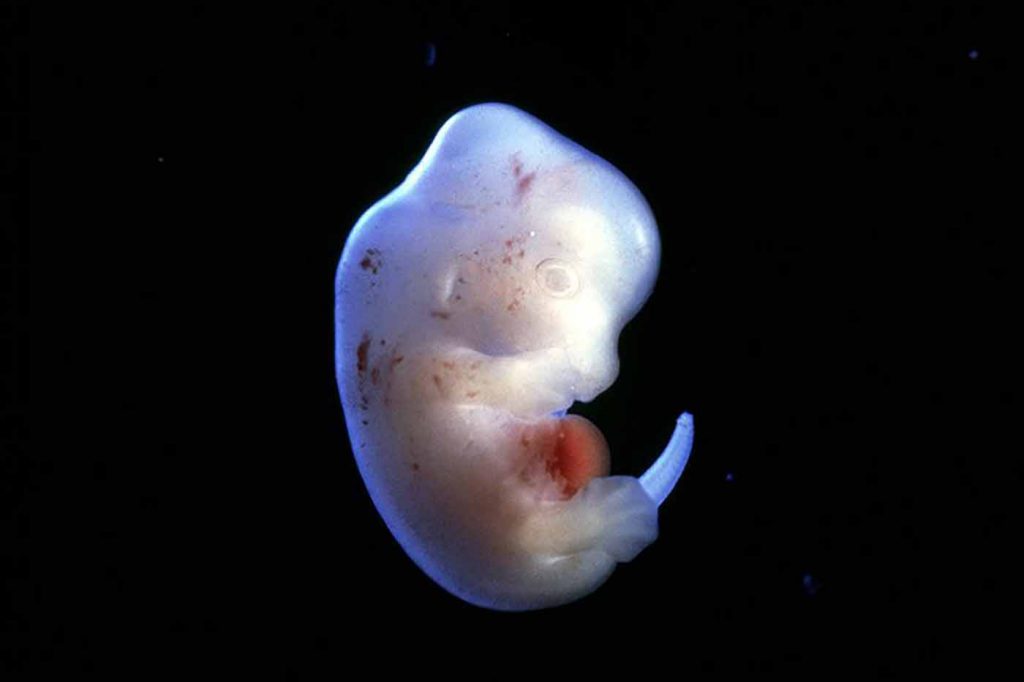
Сергей Медведев: Как я понимаю, в геноме три миллиарда букв. Нам известен код – что мы можем сделать с этим кодом? Это некая поваренная книга жизни, мы теперь можем приготовить человека, гомункула из пробирки?
Жизнь умеет воспроизводить себя по рецептам, которые содержатся в этой книге
Михаил Гельфанд: Это поваренная книга жизни в том смысле, что жизнь умеет воспроизводить себя по рецептам, которые содержатся в этой книге. Мы не умеем, мы в этом смысле плохие повара.
Вообще, эта метафора с расшифровкой и прочтением генома не очень удачна, потому что расшифровка предполагает понимание, а мы пока понимаем довольно плохо. Ту молекулу наследственности ДНК, которая была в живой клетке, а потом в пробирке, мы научились воспроизводить в компьютере, мы знаем, в каком порядке сочетаются эти буквы в этой молекуле. Но понимание смысла – это немножко другая вещь.
Биоинформатика появилась как самостоятельная наука ровно тогда, когда биология постепенно начала превращаться из науки, работающей с отдельными объектами, в науку, в которой очень много данных. В этот момент появляется необходимость хранить, осмыслять, анализировать эти данные и что-то с ними делать.
Сергей Медведев: Это примерно какие годы?
Михаил Гельфанд: В 1977 году разработали методы определения последовательности ДНК (я специально говорю: не "расшифровки", а "определения последовательности"). Биоинформатика начала зарождаться, по-видимому, в начале 80-х. Мне страшно повезло: когда я в 1985 году окончил университет, была такая чудесная область, в которой не надо было ничего учить, она начиналась с нуля, можно было просто брать и делать. Так очень редко бывает в истории.
Сергей Медведев: В ней больше применяются математические методы?
Биоинформатика начала зарождаться в начале 80-х
Михаил Гельфанд: Методы в ней математические в следующем смысле: думать надо. Там в каких-то местах есть красивые алгоритмы, красивая статистика, но, в принципе, математика там достаточно тривиальная, никаких математических волшебных палочек там нет. Нужен навык держать в голове много всего и пытаться это по-разному объяснять, и второй навык – задавать простые вопросы. Вот в этом смысле мне было очень полезно математическое образование, даже не столько, может быть, образование, сколько общение с моим дедом Израилем Моисеевичем Гельфандом, который был математиком и очень много работал в экспериментальной биологии.
Сергей Медведев: Сейчас записан геном, определена последовательность – что мы можем из этого сделать? Я слышал, есть новая технология: мы можем взять какую-то цепочку генов и починить ее, вставить вместо нее хорошую. То есть мы можем оперировать этими буквами?
Михаил Гельфанд: CRISPR – это техника генной инженерии, одна из очень продвинутых, очень современных технологий, которая позволяет делать весьма точные и конкретные манипуляции.
У людей просто появилось больше возможностей. В принципе, вставлять и вынимать гены люди умели и раньше, просто это было тяжелее экспериментально, не любые манипуляции были технически осуществимы. Сейчас расширился набор инструментов. Можно было строить дома, как в Спарте, только топором, а теперь есть еще пила и даже лобзик, вы можете выпиливать какие-то красивые наличники. В этом смысле технологическое продвижение очень большое, но пока что не очень содержательное. Какие-то вещи мы понимаем: что есть простая моногенная болезнь, в которой сломан один-единственный ген, – понятно, что если его починить, то будет нормальный эмбрион.
Сергей Медведев: И это уже лечится?
У людей просто появилось больше возможностей
Михаил Гельфанд: Нет, это не лечится, нельзя манипулировать с человеческими эмбрионами – это просто законодательно запрещено.
Сергей Медведев: Но, как я понимаю, это движется. В Англии разрешили – с эмбрионами до 11 дней…
Михаил Гельфанд: В Китае даже спрашивать никого не будут. Вы не можете затормозить каток, подкладывая под него черепах: черепах жалко, но катку ничего не будет. В этом смысле, конечно, это будет двигаться, но человечеству надо это осмыслить. Это действительно серьезная вещь, которая требует осмысления.
Она не первая. Когда в середине 70-х годов только началась генная инженерия, когда стало ясно, что геномами можно манипулировать (тогда еще бактериальными), то уже была серьезная проблема: например, боялись, что случайно сделают какую-нибудь супербактерию, и она всех съест. Были специальные конференции, где вырабатывались правила, что мы делаем, а что не делаем. Всякий новый набор инструментов расширяет возможности, увеличивает ответственность, и он должен быть осмыслен.
Сергей Медведев: Ставит этические вопросы…
Михаил Гельфанд: А если говорить про биоинформатику, возвращаясь к тому, о чем вы спросили, то там немножко другая история. Там есть два аспекта. Оказалось, что мы можем отвечать на довольно многие классические биологические вопросы просто в компьютере.
Я много занимаюсь геномикой бактерий. Есть очень много бактерий, с которыми в их жизни был сделан один опыт, а именно: определили последовательность генома. Мы про них довольно много знаем: что они едят, что не могут есть, как они дышат, что им надо добавлять в среду, без чего они не могут выжить, а сами сделать не могут, и так далее.
Сергей Медведев: Насколько проще геном бактерии по сравнению с геномом человека?
Всякий новый набор инструментов расширяет возможности и увеличивает ответственность
Михаил Гельфанд: Это не так критично. У нас с кишечной палочкой 30% общих генов. По количеству генов типичная бактерия – это тысячи, а человек – 25 тысяч.
Сергей Медведев: Вы целиком знаете, какой ген за что отвечает у бактерии?
Михаил Гельфанд: Не целиком, но много знаем.
Сергей Медведев: Гораздо больше, чем о человеке?
Михаил Гельфанд: В процентах – конечно.
Вторая вещь, которая появилась (и это, опять-таки, связано с технологическим развитием в экспериментальной биологии) и требует осмысления в биоинформатике, – это то, что мы можем смотреть на клетку целиком. Классическая вещь: аспирант изучает какой-то белок, он знает партнеров этого белка, знает, как этот белок взаимодействует с ДНК, если он с ней взаимодействует, знает, когда включается и когда выключается ген этого белка. Это такая полноценная диссертация, несколько научных статей про один белок. А потом появляются методы, которые позволяют отвечать на те же самые вопросы для всех белков сразу. У нас впервые появляется интегральная картина того, как устроена клетка; она сейчас очень несовершенна.
Сергей Медведев: Есть белок, который вам незнаком, но вы можете предсказать, глядя на его геном…
У нас с кишечной палочкой 30% общих генов
Михаил Гельфанд: Это два разных вопроса. Мы умеем предсказывать функции белков, не делая с ними никаких экспериментов. Это красивая биоинформатика, основанная на всяких эволюционных соображениях.
Сергей Медведев: Основанная на его генном профиле?
Михаил Гельфанд: Белок – это то, что закодировано в гене, поэтому лучше говорить про ген: основанная на том, с кем этот ген лежит рядом, на кого этот белок похож из уже хотя бы немножко известных, на том, как он регулируется, когда он включается и выключается.
Сергей Медведев: То же самое, наверное, можно сделать и про человека?
Михаил Гельфанд: Это труднее. Технически – можно.
Сергей Медведев: Посмотреть на геном какого-то человека на эмбриональном уровне и сказать: вырастет гений или вырастет Даун.
Михаил Гельфанд: Это история про то, что функция белка вообще неизвестна, про нее вообще ничего не знали, и мы можем ее предсказать. А то, о чем вы говорите, это известный набор белков, но с какими-то вариациями – это немножко другая история.
Сергей Медведев: Человек состоит из известных белков.
Михаил Гельфанд: Частично – известных, частично – нет. Оказалось, что у нас очень много разнородной информации по поводу того, как устроена клетка. Информация очень несовершенная, каждый отдельный маленький фактик легко может оказаться неверным, но в совокупности они все-таки правильные. И вот из этого можно пытаться описывать клетку целиком.
Молекулярную биологию очень долго ругали философы за то, что это редукционистская наука
Молекулярную биологию очень долго ругали философы за то, что это редукционистская наука. Вот вы смотрите слона по частям: кто-то изучает ногу, кто-то – хвост, кто-то – хобот, и никакой целостной картинки не складывается. Теперь она впервые начинает складываться. Одним из парадоксальных результатов этого является то, что наши знания и понимание в абсолютном смысле увеличиваются очень быстро. В биологии прогресс потрясающий: мы знаем намного больше, чем знали 10 или 20 лет назад, даже не в разы, а на порядки больше.
Но еще быстрее увеличивается область незнания. То есть относительное наше знание на самом деле, по-моему, убывает, так как становится понятно, что есть такие просторы, про которые десять лет назад нам просто в голову не приходило, что такое бывает. А теперь мы видим, что это есть, но не знаем, что с этим делать. Вот это страшно прикольно.

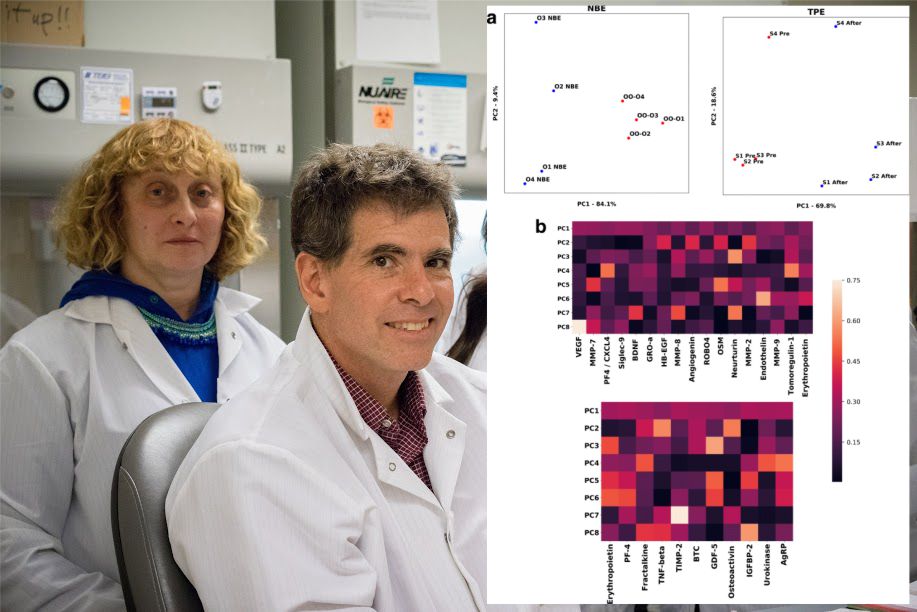
Михаил Гельфанд
Кто будет Даун – это понятно: лишняя хромосома. А вот кто будет, а кто не будет гением, мы не умеем предсказывать, и слава богу. Мы даже рост плохо умеем предсказывать.
Сергей Медведев: Не идет накопление этой информации?
Михаил Гельфанд: Идет, конечно.
Сергей Медведев: Можно ли, скажем, сопоставлять поведение человека, его профиль в соцсетях с его генетическим профилем?
Михаил Гельфанд: Про это я не знаю, а вот психологические черты частично определяются геномом, и их можно немножко предсказывать.
Сергей Медведев: Частично – геномом, частично – обществом.
Психологические черты человека частично определяются геномом, и их можно немножко предсказывать
Михаил Гельфанд: Обществом, какими-то жизненными обстоятельствами... В генетике это разработанная вещь, вы можете количественно оценить вклад генетических факторов в тот или иной признак. Давайте возьмем кого-нибудь одного – меня. У меня во всех клетках геномы одинаковые, а клетки у меня разные.
Сергей Медведев: То есть в какой-то момент геномы понимают, в какую клетку им развиться?
Михаил Гельфанд: В какой-то момент клетка понимает, что она должна стать предшественником эпителия или нервной системы, или печенки, или чего-то еще. После первых делений все клетки одинаковые, гены в них работают одинаково, а потом начинают работать по-разному. Ключевая вещь на самом деле – не сами гены: у меня и у шимпанзе 50% белков одинаковые, а те, что разные, отличаются на одну букву.
Сергей Медведев: То есть вопрос в том, где та программа, которая в какой-то момент говорит клетке, что она должна развиться в человека или в шимпанзе, а в человеке – в мозг или в печень.
Михаил Гельфанд: Он там же, в генах, но ключевая вещь – не сами гены, а то, как они включаются и выключаются. И вот это – самое интересное, что сейчас происходит в биологии.
Сергей Медведев: А есть программа, которая включается и выключается?
Есть мутации, когда у дрозофил вместо усика вырастает нога
Михаил Гельфанд: Конечно. У дрозофил это хорошо известно. Дрозофила простая, зародыш у нее тоже простой… Нет, дрозофила сложная, но ранние этапы ее развития очень хорошо описаны именно количественно на уровне моделей. Например, можно предсказывать результаты мутаций. Есть мутации, когда у дрозофил вместо усика вырастает нога. При этом известно, в каком гене мутация, что сломано, и это можно смоделировать – как ошибаются клетки-предшественники.
Сергей Медведев: А можно это починить с новыми технологиями?
Михаил Гельфанд: Можно, но только у зародыша. Когда выросла нога или лишняя пара крыльев, уже не починишь.
Сергей Медведев: Что это может принести в практическом смысле? Скажем, то, что интересует каждого человека, – борьба с раком… C этой потрясающей технологией CRISPR китайцы, кажется, пытаются бороться с раком легких. Как я понимаю, в этой технологии бактерия, когда она видит у себя фрагмент сломанной ДНК, берет кусочек у здоровой бактерии и замещает сломанную цепочку здоровой.
Михаил Гельфанд: Да, только интересный вопрос, что происходит со здоровой бактерией… Нет, не так. CRISPR/Cas-системы – это бактериальный иммунитет, немножко другая вещь. Когда бактерию заражает вирус, если он не успел ее убить, там начинается война, вирус переключает какие-то бактериальные системы, ломает бактериальную генетическую программу и переключает бактерию на производство новых вирусов. Собственно, все вирусы так делают: и бактериальные, и человеческие, и какие угодно. Есть система, которая позволяет бактерии, если вирус не успел ее убить в самом начале, вырезать кусочек ДНК вируса и использовать как образец при следующей атаке такого же вируса.
Сергей Медведев: Бактерия сама себя прививает этим вирусом.
Типичный признак рака – когда гены, которые работают на эмбриональных стадиях, начинают работать во взрослых тканях
Михаил Гельфанд: В каком-то смысле – да. А дальше оказалось, что есть белок, который способен вырезать кусок и целенаправленно его куда-то вставить, и вы этот же самый фермент можете использовать для целей генной инженерии.
Про такую терапию рака я не очень понимаю: когда у вас есть миллиарды клеток, как вы собираетесь в каждую из них встроить правильную систему? Я не понимаю, как это технически сделать. Это можно делать для лечения генетических дефектов на стадии эмбриона, когда там одна клетка.
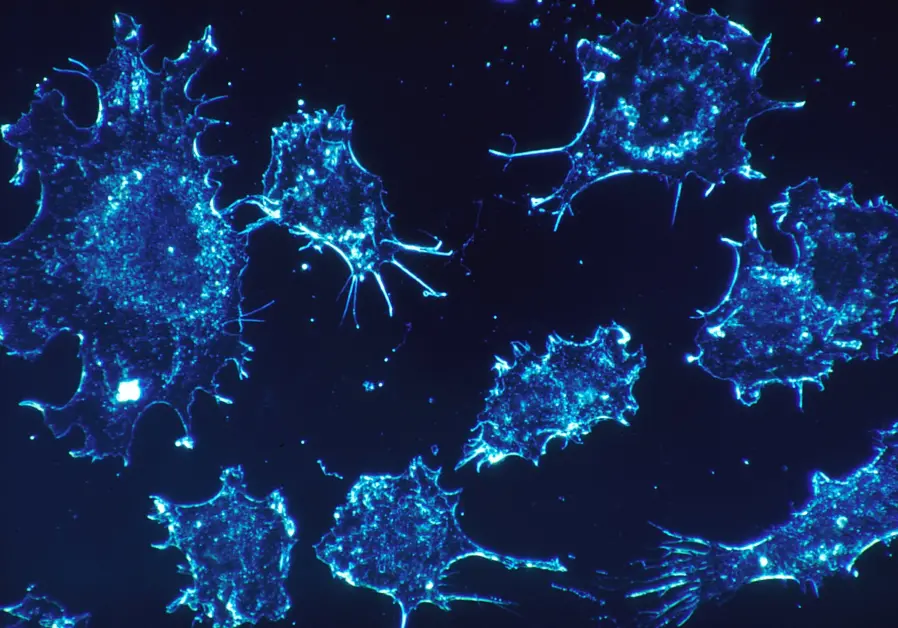
С раком история немножко другая, там действительно очень существенный прогресс. Стало ясно, что то, что мы принимали за одну и ту же болезнь, это на самом деле на молекулярном уровне – разные болезни, и мишени для терапии тоже должны быть разные. Рак сначала классифицировали просто по месту: был рак легких, рак желудка, рак кожи. Потом началась гистология. Когда стали смотреть на структуру опухоли, на то, из каких клеток она состоит, начались диагнозы типа "мелкоклеточный рак легких". Потом началась биохимия, стали смотреть какие-то маркеры, это раздробилось еще дальше.
А теперь мы можем посмотреть, какие, собственно, произошли мутации. Вы берете образец из раковой опухоли и образец из такой же нормальной ткани, и смотрите, чем они отличаются. Они очень сильно отличаются, потому что при раке все ломается, ошибки начинают накапливаться очень быстро. Есть специальные термины – "водители" и "пассажиры": какие-то из этих ошибок – пассажиры, они получились случайно, а какие-то были водителями, они, собственно, и привели к перерождению.
Там применяются совершенно практические вещи, потому что, например, ясно, что какие-то раки, которые считали одной болезнью, надо лечить по-разному. И наоборот, если у вас внешне разные раки, но у них одна и та же молекулярная поломка, то вы можете лекарство, эффективное против одного, пытаться использовать против другого.
Сергей Медведев: Это поломка на генетическом уровне, выбит какой-то ген?
Михаил Гельфанд: Или выбит, или, наоборот, начал работать слишком интенсивно. Типичный признак рака – когда гены, которые работают на эмбриональных стадиях, начинают работать во взрослых тканях. Эти клетки начинают бесконтрольно делиться. Довольно многие раки – это на самом деле перерождение, деградация назад во времени.
Биоинформатика – это не наука в том же смысле, в котором не является ею электронная микроскопия, – это набор приемом
Я сразу хочу подчеркнуть: я не медик, я про это знаю как биолог и человек, немножко читающий обзоры. Я просто всегда очень боюсь разочаровывать людей. Всегда есть баланс между успехами в науке и практическим вопросом – для тех, кому завтра идти лечиться. Это экспериментальные вещи. Есть единичный пример, когда это работало. Но ясно, что именно в этом направлении все и будет происходить.
Сергей Медведев: Если посмотреть медицинское применение, вы видите, что уже пойдет генная инженерия, генная терапия? Сейчас, насколько я понимаю, на отдельных аутоиммунных заболеваниях видно, что какой-то один ген сломан.
Михаил Гельфанд: Это, скорее, наоборот, дефект иммунной системы, выбитая иммунная система. Это пытаются лечить.
Сергей Медведев: Иммунодефицит на генном уровне?
Михаил Гельфанд: Это связано со спецификой иммунной системы. Там клетки все время делятся, все время возникают новые клоны. Даже если у вас все дефектное, но вы сделали небольшое количество починенных клеток-предшественников, то они могут заместить всю систему иммунитета, породить ее заново. Это связано как раз со спецификой того, как вообще устроена иммунная система. Она в этом смысле потрясающе пластична.
Сергей Медведев: Бактерия создала себе некую прививку, иммунитет?
Михаил Гельфанд: Да, но там немножко другое. Опять-таки, когда речь идет об иммунодефиците, это означает, что вообще нет каких-то классов клеток, потому что сломан тот ген, который должен работать, когда эти клетки созревают. Если вы почините этот ген каким-то предшественникам, они созреют в эти клетки, то они дадут начало всей этой большой иммунной картине.
Сергей Медведев: Есть же еще, как я понимаю, вычислительная эволюционная биология. Вы можете откатиться назад и посмотреть ген древнего человека?
Наши отличия от мышки начинаются на первых стадиях эмбриона, а потом уже все фиксируется
Михаил Гельфанд: Это почти самое интересное. Биоинформатика – это не наука в том же смысле, в котором не является ею электронная микроскопия, – это набор приемов. Научная часть биоинформатики, это, во-первых, то, что связано с биологией развития, а во-вторых, это молекулярная эволюция, и там можно делать разные чудесные вещи.
Мы гораздо лучше понимаем, как это происходило. Наши отличия от мышки начинаются на первых стадиях эмбриона, а потом уже все фиксируется. Одни и те же гены работали немножко в разных комбинациях. Эта мечта описать разнообразие животных с пониманием того, как они возникали, идет еще от Геккеля. Геккель многое подтасовывал, за что его и ругают, но сама по себе идея очень правильная. Чтобы понять отличие человека от мыши, надо смотреть не взрослого человека и взрослую мышь, а эмбрионы на первых стадиях. Это сейчас становится реальным.
Вторая вещь: мы понимаем, кто кому родственник, просто сравнивая геномы. Понятно: чем меньше отличий, тем ближе родство. Это очень простая идея, ее можно алгоритмизировать. Наши представления об эволюции живых существ вообще довольно сильно поменялись. Традиционно грибы всегда изучали на кафедре низших растений, а на самом деле грибы никакие не низшие растения, а наши ближайшие родственники. Нам с грибами цветочки – двоюродные. Из этого следует, что многоклеточность возникала много раз независимо, а это уже очень принципиальный вопрос. Когда мы с вами учились в школе, были бактерии, потом были простейшие, а потом простейшие начали слипаться и получились многоклеточные, а потом многоклеточные разделились на растения и животных. Были какие-то низшие растения, грибы и высшие растения – розы и лютики. А на самом деле не так: было много разных одноклеточных, и в этих разных линиях одноклеточных несколько раз независимо возникала многоклеточность.
Сергей Медведев: Человек как высшая форма многоклеточности?..
Грибы никакие не низшие растения, а наши ближайшие родственники
Михаил Гельфанд: Я не знаю, в каком смысле высшая. Если смотреть по разнообразию тканей, то все млекопитающие в одну цену. Если смотреть по сложности нервной системы, то нас надо сравнивать с осьминогами. Но если кому-то приятно быть антропоцентристом, то на здоровье, я не возражаю.
Наше представление о происхождении человека очень сильно поменялось. В каждом из нас 2% неандертальца, а еще были денисовцы (денисовский человек), про которых вообще никто не подозревал. На самом деле в Евразии 40 тысяч лет назад было три независимых ветки человечества, они скрещивались во всех сочетаниях, и остатки этих скрещиваний мы видим в геноме.
Сергей Медведев: Это вы все берете по останкам того, что осталось на стоянках?
Михаил Гельфанд: Это старая ДНК и анализ современной ДНК разных людей. По-моему, это очень здорово. Это очень сильно перекашивает мою картину мира.
Сергей Медведев: Михаил, вы нас озадачили. 2% неандертальцев, зато очень много общего с грибами, с цветами… Действительно, здесь идет речь о кубиках, из которых устроена жизнь. Сейчас, как я понимаю, вы эти кубики комбинируете в разном порядке, смотрите, какие признаки произошли и в онтогенезе, и в филогенезе, как развился эмбрион отдельного человека, как вообще развилась жизнь на Земле.
Михаил Гельфанд: Да. Мы делаем это в компьютере, а экспериментаторы делают в клеточках.
Мы живем в восхитительное время!
Сергей Медведев: Мы живем в восхитительное время! Будем надеяться, что эти эксперименты приведут и к созданию лекарств от рака и СПИДа.
Михаил Гельфанд: Вообще-то лекарство от рака уже создали.
Сергей Медведев: Я имею в виду понимание механизмов действия.
Михаил Гельфанд: А с диагнозом СПИД люди живут и живут на современных лекарствах.
Сергей Медведев: Вопрос не о лекарствах, а о том, чтобы лечить это на генном уровне. Это дальнейшее пожелание.
8.04.2017 Источник: svoboda.org