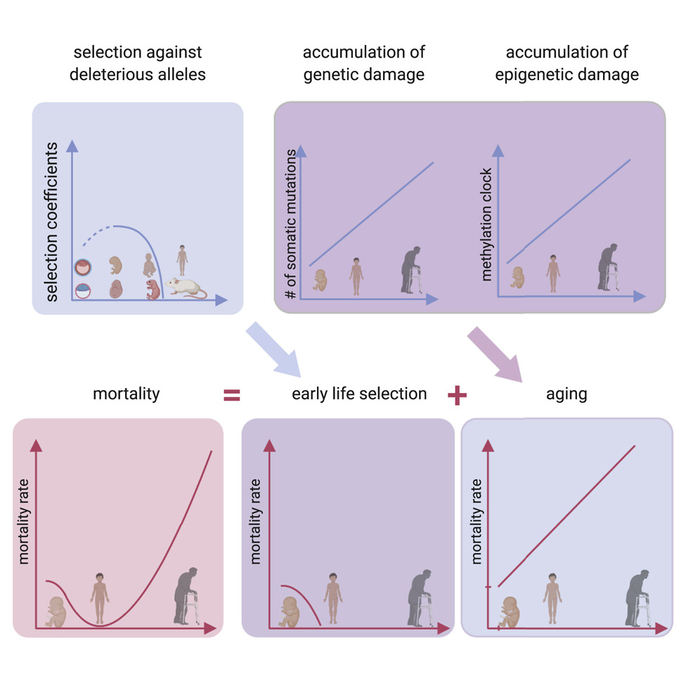
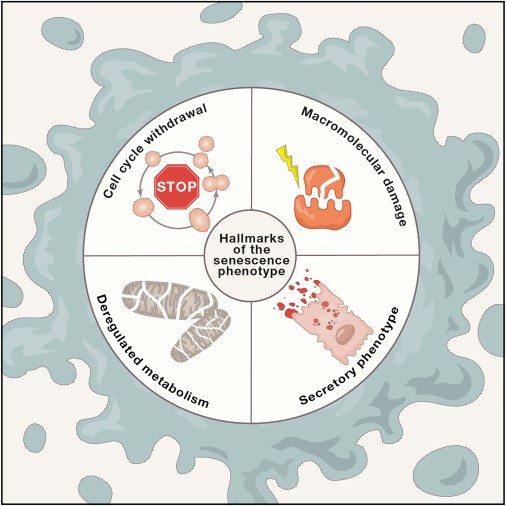
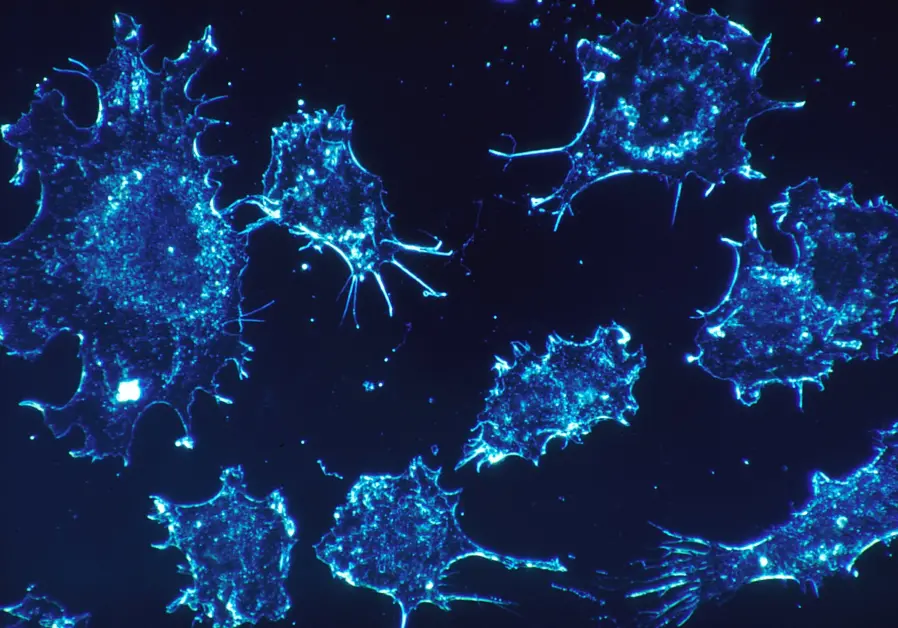
Представляем вашему вниманию традиционный полугодовой обзор самых важных новостей фарминдустрии и медицинского биотеха, подготовленный нашим экспертом Ильёй Ясным.
Успехи CAR-T
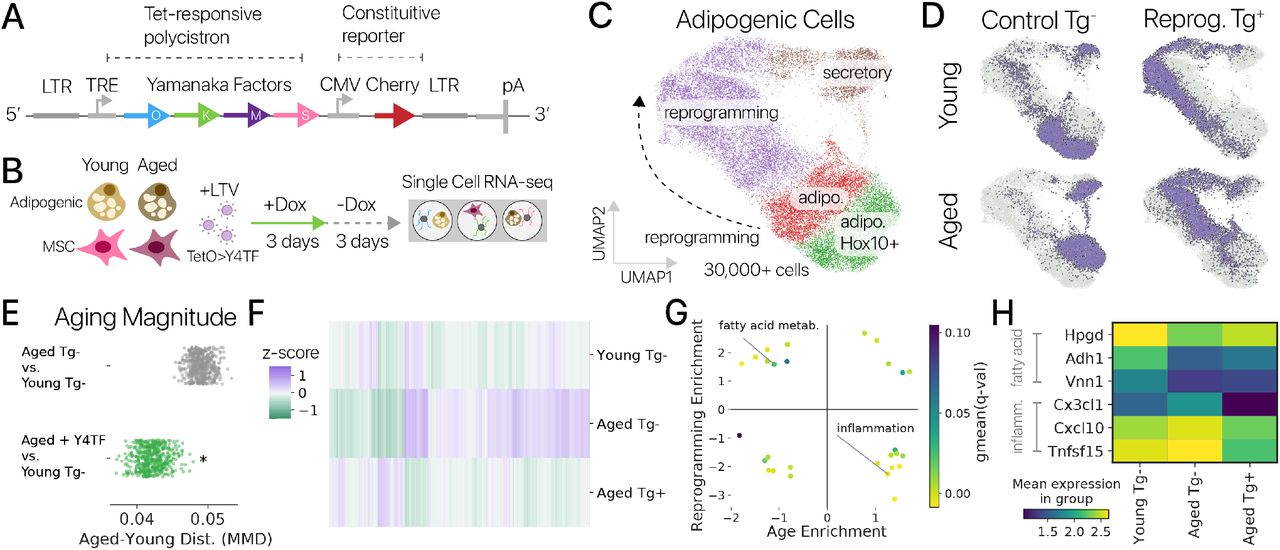
В области CAR-T, о которых мы неоднократно писали, за последние полгода произошло несколько громких событий. Компания Juno Therapeutics остановила свою программу по CAR-T в связи со смертью 7 пациентов в 2016 году. Ближе всех к финишу в гонке за регистрацией FDA компании Kite Pharma и Novartis International AG, продолжающие подогревать интерес публики новостями об успехах.
Kite в феврале сообщила о 6-месячных данных исследования у пациентов с агрессивными В-клеточными лимфомами, устойчивыми к терапии. Более трети пациентов вылечились после единственной инъекции препарата, почти все были живы. Это удивительный результат, так как обычно только половина таких пациентов доживает до 6 месяцев. Картину несколько омрачила смерть одного из пациентов по причине отёка мозга (как и у Juno), однако компания и регулятор утверждают, что пациент был крайне тяжёлый. Заседание комиссии FDA по рассмотрению заявки на регистрацию назначено на 29 ноября.
Похожие данные по эффективности своего продукта опубликовала и компания Novartis, причём в её исследовании пока не наблюдалось случаев нейротоксичности. Заседание FDA ожидается в конце сентября, примерно на 2 месяца раньше Kite.
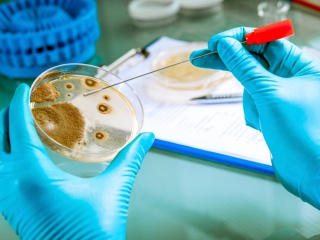
Kite несколько превосходит Novartis по скорости производства продукта. Сейчас производство этих продуктов занимает 3—4 недели и стоит десятки тысяч долларов. Связано это с тем, что клетки отбирают у самого пациента, изменяют их методами генетической инженерии и вводят обратно пациенту. Для части пациентов вообще невозможно получить продукт, и индивидуальный подход является причиной такой высокой цены.
Для решения этой проблемы компания Cellectis разрабатывает клетки, взятые не у самого пациента, а из донорского материала. Стоимость этой технологии, как обещает компания, не превзойдёт $10 000. Правда, клинические данные пока получены только на 2 пациентах, из которых у одного возникла реакция «трансплантат против хозяина» — к счастью, с ней удалось справиться.
Все перечисленные продукты направлены против одного и того же белка на поверхности предшественников В-клеток — CD19, поэтому применяются только у пациентов с В-клеточными лимфомами и лейкемиями. На конференции клинической онкологии ASCO (American Society of Clinical Oncology) в июне впервые были представлены данные по продуктам против ВСМА — другого белка, характерного для множественной миеломы. Долгое время лидером в этой области являлись известные американские компании bluebird bio (капитализация которой составляет около 4 млрд долл., несмотря на отсутствие продуктов на рынке) и Celgene Corporation (один из гигантов биотеха), но в этом году в круг конкурентов внезапно ворвался китайский стартап Nanjing Legend Biotech, доложивший о 100% объективных ответов на терапию 35 резистентных пациентов с множественной миеломой. 5 пациентов наблюдаются уже год без признаков болезни. Раньше почти никто не слышал об этой компании, и есть предположение, что это не последний сюрприз, который преподнесёт китайский биотех.
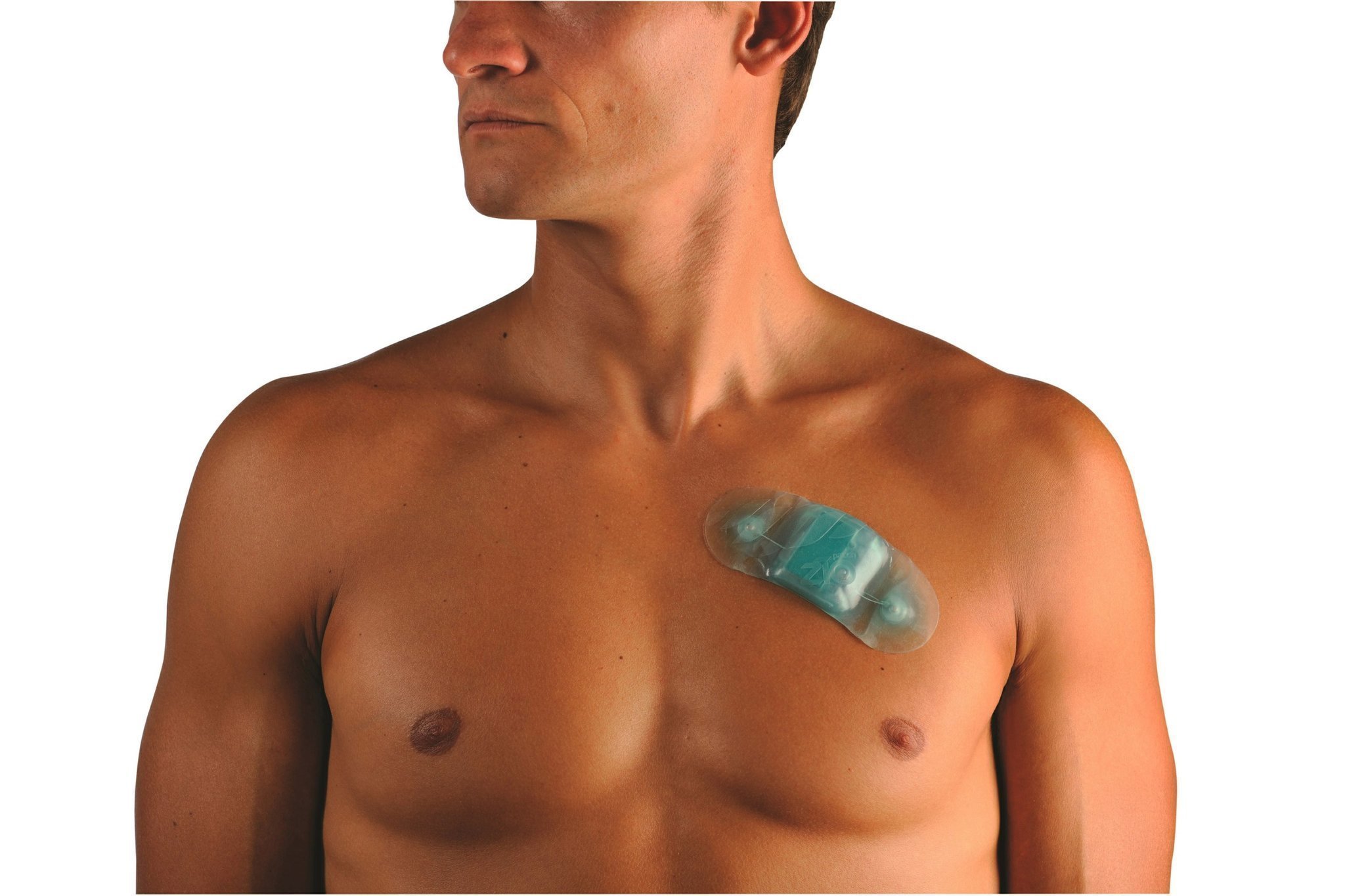
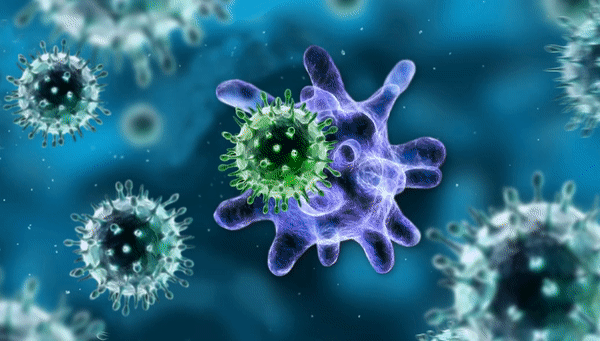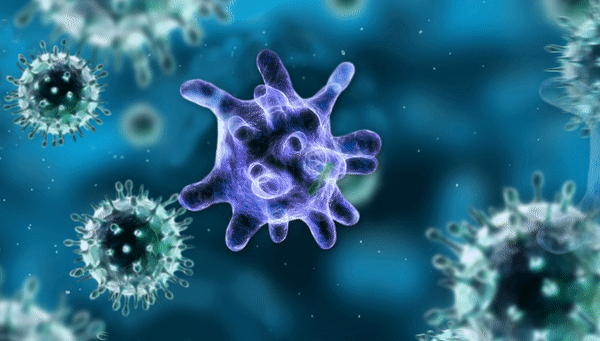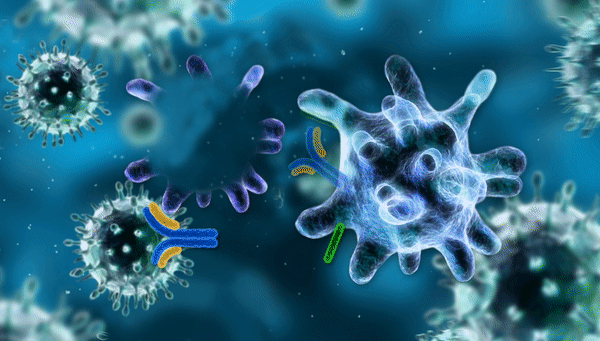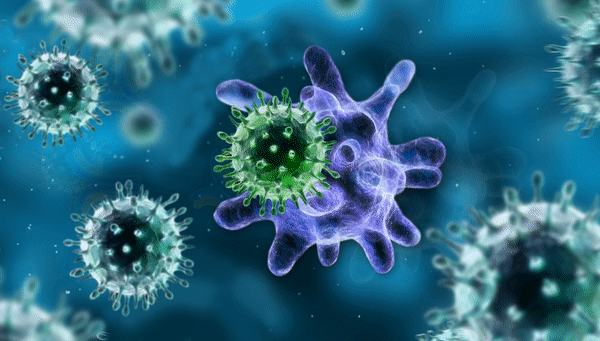
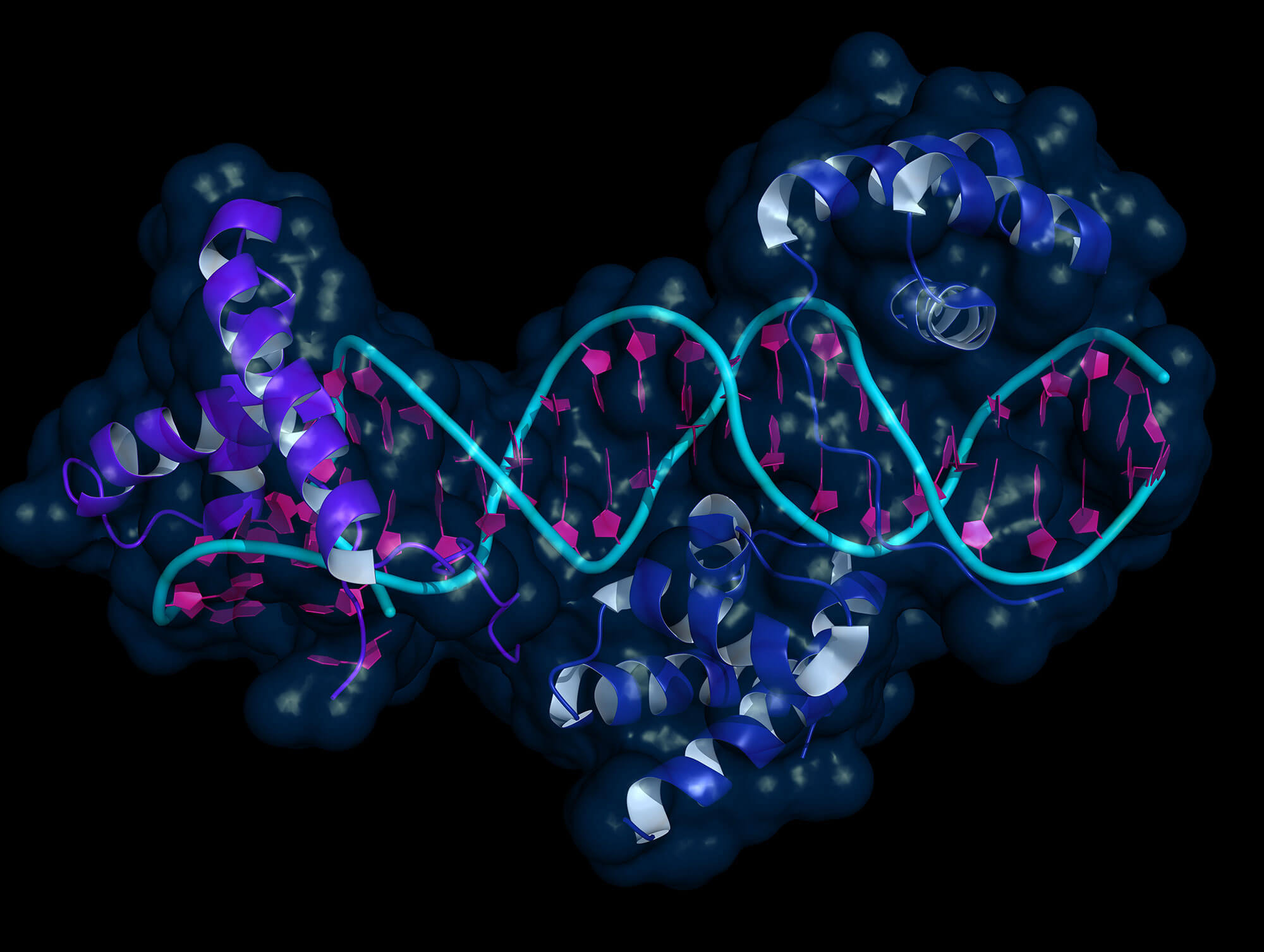
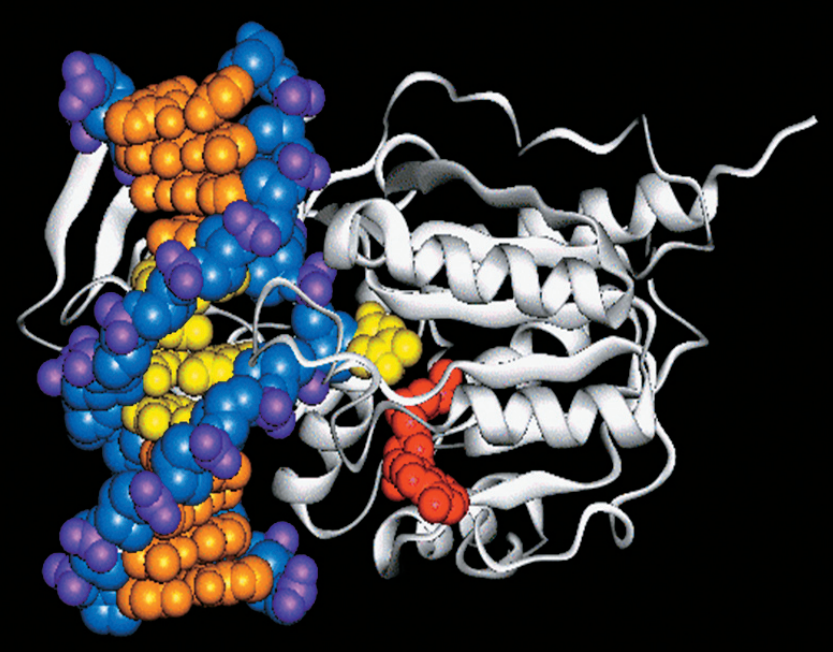
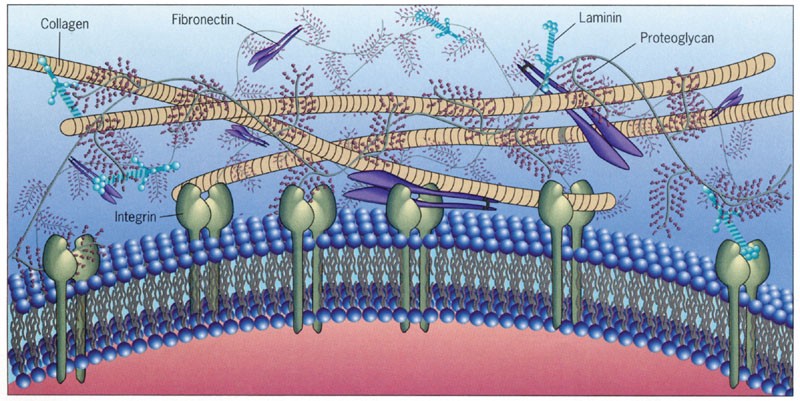
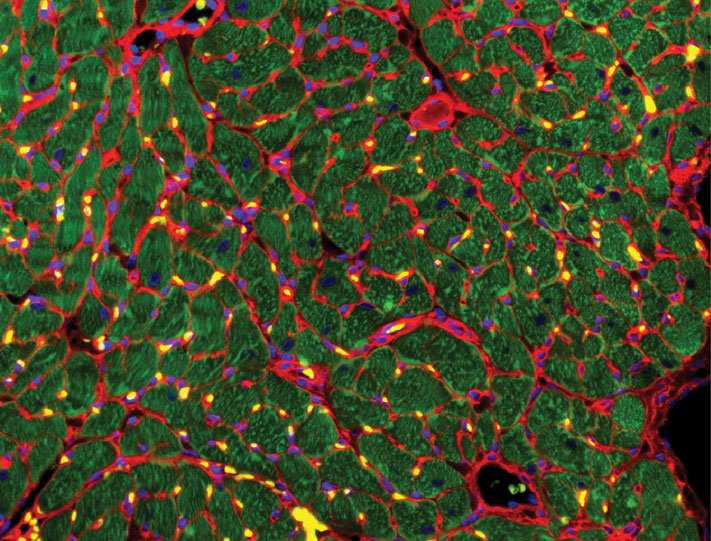
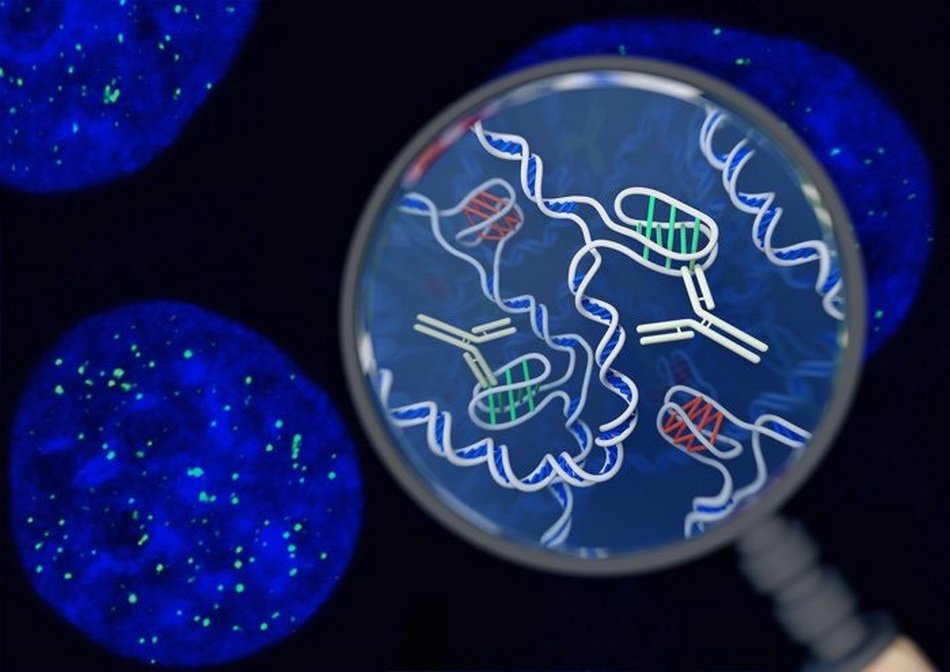
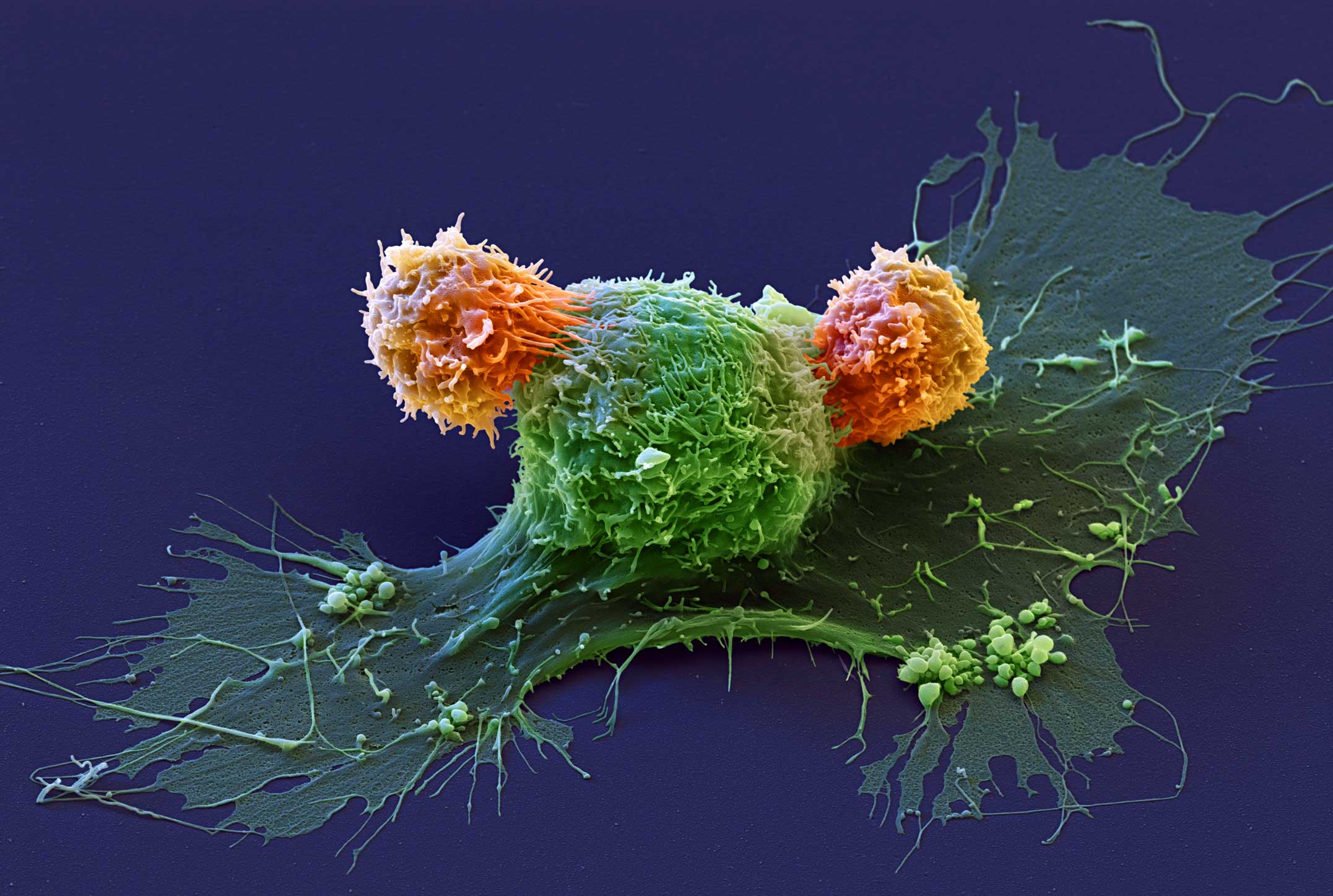 Рисунок 1. Химерный рецептор показан как зелёно-сине-красная «вилка» на поверхности Т-клетки. Он связывается с жёлтым белком CD19 на поверхности опухолевой клетки, что приводит к активации Т-клетки, её многократному делению и атаке на опухоль. Химерный рецептор получен генно-инженерным способом, и ему не нужны клетки-посредники (APC — antigen presenting cells на врезке слева) для обучения атаке на опухоль, в отличие от обычных Т-клеток.
Рисунок 1. Химерный рецептор показан как зелёно-сине-красная «вилка» на поверхности Т-клетки. Он связывается с жёлтым белком CD19 на поверхности опухолевой клетки, что приводит к активации Т-клетки, её многократному делению и атаке на опухоль. Химерный рецептор получен генно-инженерным способом, и ему не нужны клетки-посредники (APC — antigen presenting cells на врезке слева) для обучения атаке на опухоль, в отличие от обычных Т-клеток.
CAR-T, скорее всего, займут своё место в лечении пациентов с гемоонкологическими заболеваниями (которые иногда неправильно называют «раки крови»), однако успехов в лечении сóлидных опухолей (таких как рак молочной железы, лёгких, простаты) пока нет, несмотря на многочисленные попытки.
Генная модификация людей
Панель Национальной академии наук США (United States National Academy of Sciences) в феврале выдала беспрецедентную рекомендацию о том, что в исключительных случаях будет разрешено модифицировать зиготу человека для предотвращения появления на свет детей с тяжёлыми заболеваниями. Рекомендация была сделана на основе 216-страничного отчёта и содержит множество оговорок морального и технического характера. В частности, в ней говорится о том, что надёжность и безопасность технологий модификации генома, таких, как CRISPR, пока не достаточна. Поэтому генетические модификации возможны только в том случае, если нет «разумных альтернатив» и если они направлены на устранение тяжёлых заболеваний, а не, скажем, на улучшение интеллекта.
Одним из факторов, способствовавших принятию такого смелого решения, было начало клинических исследований с использованием технологии CRISPR в Китае. В США до сих нет федерального финансирования таких программ, и Штаты, безусловно, боятся отстать в этой гонке.
Противники таких решений в качестве одного из аргументов, помимо потенциальной небезопасности, высказывают опасение, что технология будет использоваться для «улучшения» параметров здоровых детей: например, клиники могут начать предлагать услугу усиления мышц с помощью технологии, предназначенной для лечения пациентов с наследственными мышечными дистрофиями. В таком случае есть опасность возникновения антиутопического разделения в обществе на тех, кто может позволить себе улучшение красоты, силы или ума за счёт новых технологий, и всех остальных. В ряде стран мира редактирование генома эмбрионов находится под запретом, включая большую часть Западной Европы.
Недавно появилась громкая новость о том, что технология CRISPR-Cas9 слишком опасна, потому что приводит к множеству мутаций в генах мышей, у которых она была применена. Правда, затем в статье были найдены методологические недостатки, из-за чего её выводы пока нельзя признать справедливыми.
Редкими генетически заболеваниями страдают миллионы людей на Земле, всего таких заболеваний насчитывается около 7000. Нынешние лекарства, как правило, облегчают состояние больных, но только для очень малой доли заболеваний, и не способны их вылечить. Будем надеяться, что через несколько лет мы услышим о первых генномодифицированных людях, избавленных от этих тяжёлых болезней с помощью новых технологий редактирования генома.
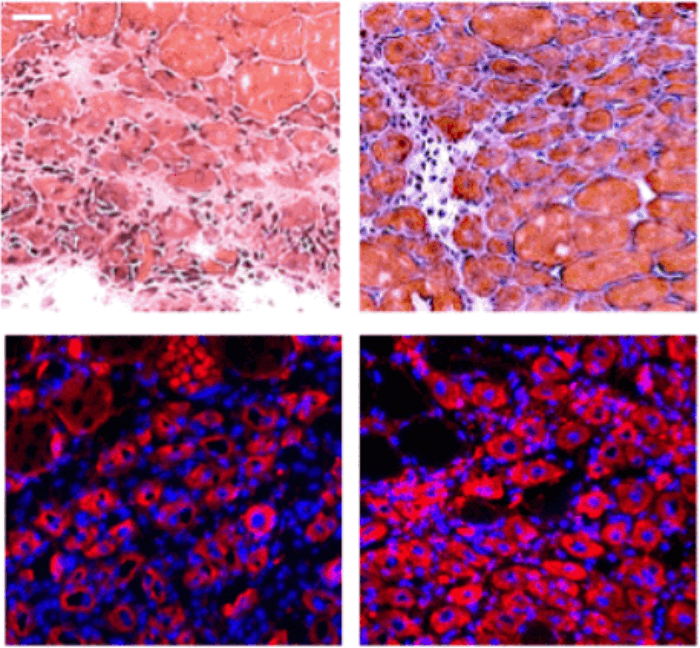
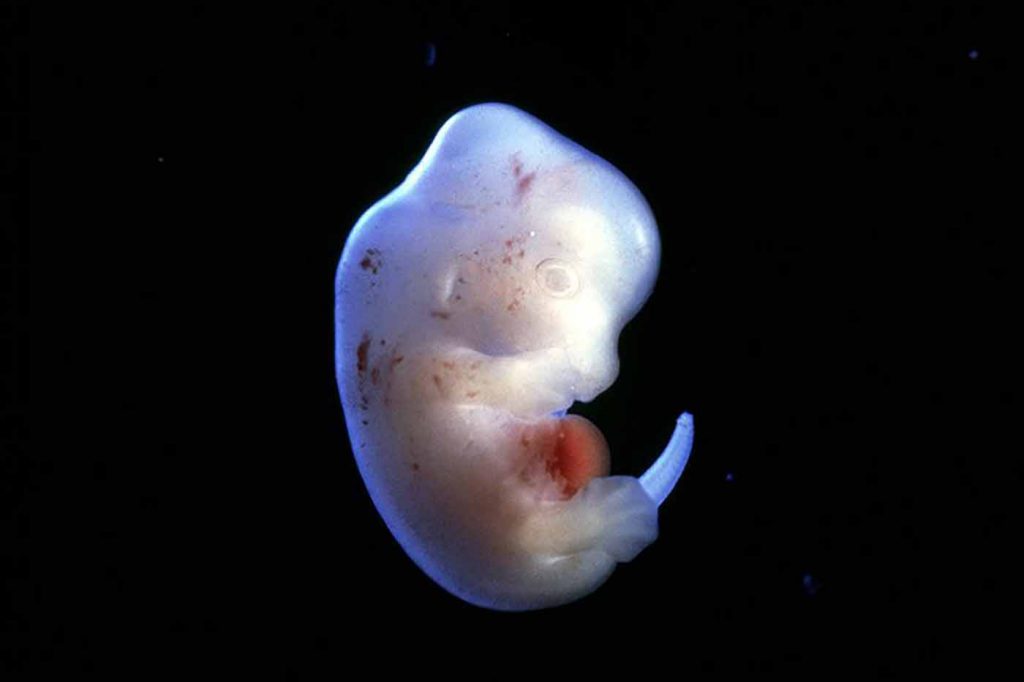
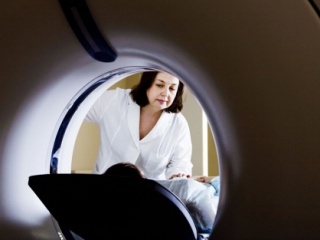
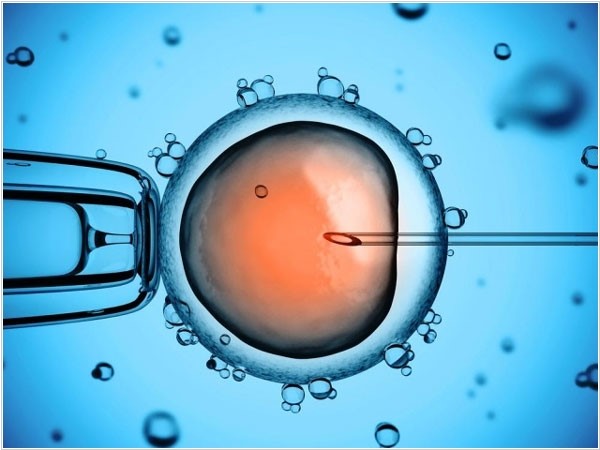 Рисунок 2. Микрофотография манипуляций с человеческой яйцеклеткой.
Рисунок 2. Микрофотография манипуляций с человеческой яйцеклеткой.
Гематоэнцефалический барьер
Гематоэнцефалический барьер (ГЭБ) — система, которая не позволяет свободно проходить большинству молекул между кровью и мозгом, и не пускает в мозг токсины и микробы — является проблемой для разработчиков лекарств. И если для многих малых молекул эта проблема решаема, для белков ситуация совсем тяжёлая — большие белковые молекулы никакими силами не могут проникнуть через ненарушенный барьер. Чтобы обойти эту проблему, предпринимаются различные ухищрения — препараты вводятся интратекально (под оболочки спинного мозга) или прямо в мозговые желудочки. Однако при таком способе введения препарат быстро выводится в кровь и часто не успевает оказать своё действие.
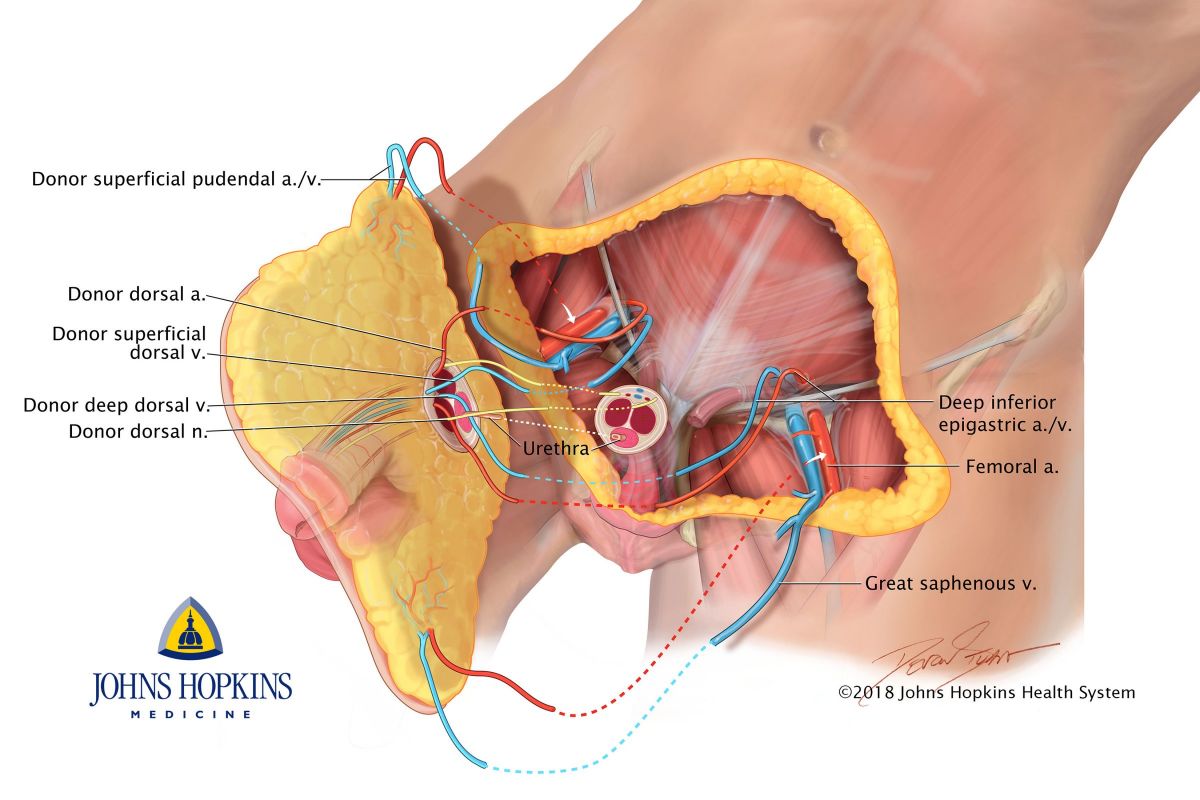
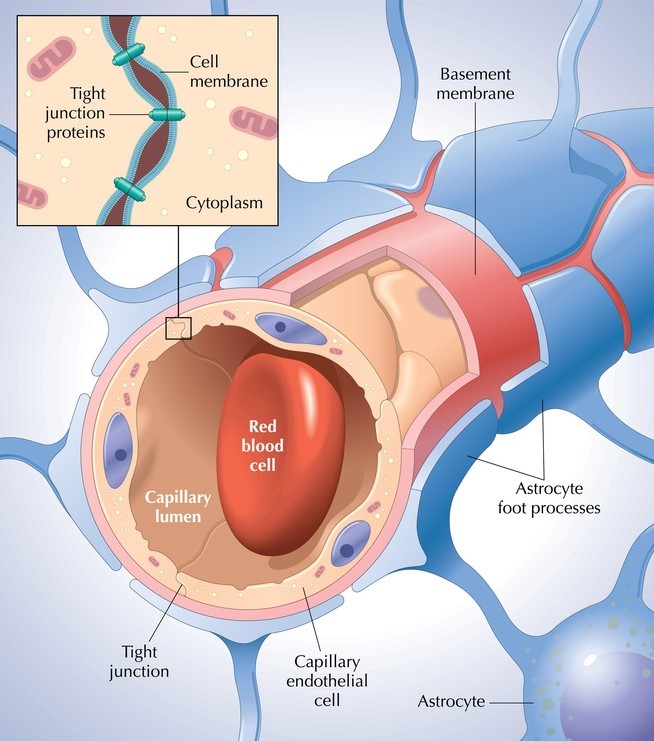 Рисунок 3. Схематичное изображение устройства ГЭБ. Барьер образован клетками эндотелия, плотными контактами между ними, мембраной капилляра, клетками мозга (астроцитами).
Рисунок 3. Схематичное изображение устройства ГЭБ. Барьер образован клетками эндотелия, плотными контактами между ними, мембраной капилляра, клетками мозга (астроцитами).
Компании ArmaGen впервые удалось не только доставить белковую молекулу за ГЭБ, но и показать в клиническом исследовании, что у пациентов с редким наследственным заболеванием — синдромом Гурлер — улучшаются показатели нервной деятельности. Синдром Гурлер (мукополисахаридоз-I H) вызван наследственным дефектом фермента идуронидазы, что приводит к накоплению в клетках полисахаридов и повреждению органов, в том числе, мозга. На рынке существует лекарство — заместительный фермент компании Sanofi Genzyme — Альдуразим (ларонидаза), который облегчает мышечные и дыхательные функции — однако не влияет на снижение когнитивных функций.
ArmaGen разработала технологию, использующую рецепторы инсулина, находящиеся в большом количестве на стенках сосудов мозга. К идуронидазе разработчики «пришили» антитело против рецептора инсулина, которое связывается с рецептором, и затем вся конструкция затаскивается за ГЭБ. Результаты 6-месячного исследования показали, что у четырёх из пяти пациентов наступило улучшение когнитивных и нейрологических параметров, а у пятого остановилось ухудшение этих функций.
Этот препарат — только первая ласточка. Если лекарство, созданное по такой технологии, будет зарегистрировано, это откроет широкие возможности для воздействия с помощью биологических молекул на мишени в мозге, что позволит более эффективно лечить не только редкие заболевания, но и болезнь Альцгеймера, Паркинсона, рассеянный склероз, метастазы в мозг и многие другие.
Новый подход к испытанию онкологических лекарств принёс плоды
Традиционно онкологических пациентов классифицировали по месту опухоли: рак лёгких, рак печени, толстой кишки и т. д. Соответственно, в зависимости от локализации опухоли пациент направляется к врачу-онкологу, специализирующемуся на данном типе опухоли, и по этому же принципу пациент включается в исследования новых лекарств.
Однако по мере накопления знаний о клеточных типах опухолей, а затем и об их генетических особенностях стало понятно, что такие разные опухоли как рак печени и меланому может объединять схожий набор генетических аномалий. И если разработать препарат, который целенаправленно действует на опухоли именно с этими аномалиями, то имеет смысл набирать в исследования пациентов с этой аномалией независимо от типа опухоли. Такие исследования были названы basket trials (от англ. basket — корзина), и в этом году дали положительные результаты первые исследования такого типа.
Препарат Keytruda (pembrolizumab, антитело против PD-1) компании Merck & Co — флагман в мире иммуноонкологии, был зарегистрирован FDA не по какому-то конкретному показанию, как все онкологические препараты до того, а для любых опухолей с микросателлитной нестабильностью (MSI, microsatellite instability). В клетках таких опухолей нарушен процесс репарации (исправления) последовательности ДНК, что приводит к накоплению мутаций во многих генах — в таких опухолях мутаций в 100-1000 раз больше, чем в обычных. Эти опухоли хуже отвечают на химиотерапию, вероятно, потому что их клетки способны к более быстрой эволюции — у них больше вариантов уйти из-под действия препаратов. Однако выяснилось, что они, наоборот, лучше отвечают на иммунотерапию. Скорее всего, причина в том, что большое количество мутантных белков опухоли вызывает формирование Т-лимфоцитов против этой опухоли, но они неактивны из-за иммуносупрессорного действия PD-1 и других подобных белков опухоли и её окружения. Введение пациенту антитела против PD-1, такого как Keytruda, снимает этот блок, и против опухоли формируется иммунный ответ, который может даже привести к полному удалению опухоли и вылечиванию пациента. Из 149 пациентов с MSI, получивших Keytruda, полный ответ наблюдался у 11, частичный — у 48. При этом у 78% ответивших пациентов опухоль не росла в течение 6 месяцев. Чаще всего опухоли такого типа встречаются у пациентов с раками толстой и прямой кишки, эндометрия, желудочно-кишечного тракта, реже — с раками молочной, предстательной, щитовидной железы, мочевого пузыря. Препарат получил регистрацию по предварительным результатам, и ему потребуются дополнительные исследования для полноценной регистрации.
Другой пример подобного рода — успешное исследование препарата larotrectinib компании Loxo Oncology. Это ингибитор семейства киназ TRK (tropomyosin receptor kinase) — сигнальных белков, мутации в которых вызывают неконтролируемый рост и повышенное выживание раковых клеток. В это исследование также набирались пациенты независимо от типа опухоли, но с мутацией в белках Trk. В итоге были набраны 50 пациентов, как дети, так и взрослые, с опухолями 17 типов. Из них 6 ответили на лечение полностью, а 32 — частично, у 91% ответивших длительность ремиссии составила не менее 6 месяцев. Однако, как известно из предыдущего опыта с ингибиторами киназ, у части пациентов к ним вырабатывается резистентность, и опухоль снова начинает расти. Поэтому компания Loxo сразу озаботилась созданием ингибитора следующего поколения, и уже испытала его на двух пациентах с резистентностью к larotrectinib.
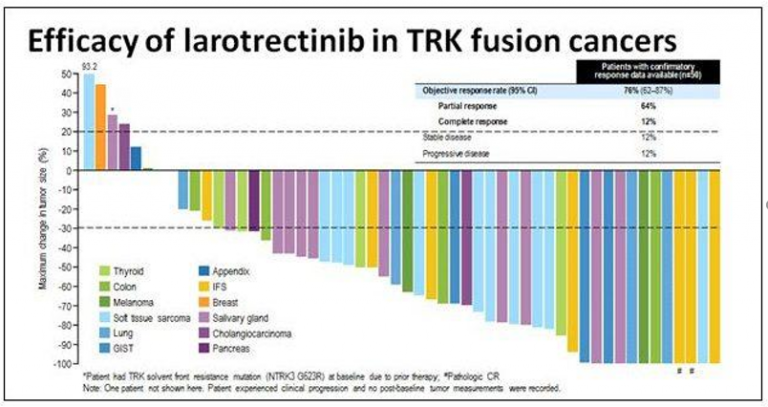 Рисунок 4. Так называемый waterfall-plot («график-водопад», гистограмма), иллюстрирующий ответы пациентов на препарат larotrectinib. Цветом обозначены различные типы опухоли, по оси ординат отложен процент изменения размера опухоли относительно начального.
Рисунок 4. Так называемый waterfall-plot («график-водопад», гистограмма), иллюстрирующий ответы пациентов на препарат larotrectinib. Цветом обозначены различные типы опухоли, по оси ординат отложен процент изменения размера опухоли относительно начального.
Такие подходы — примеры удачного применения концепции персонализированной медицины в её современном виде, когда пациентов лечат в зависимости от индивидуальных параметров их генотипа и генотипа опухоли.
Успехи профилактики сердечно-сосудистых заболеваний
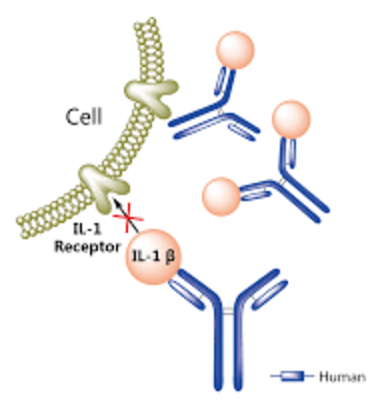 Рисунок 5. Canakinumab связывается с IL-1β и не даёт ему взаимодействовать с рецептором на поверхности клетки
Рисунок 5. Canakinumab связывается с IL-1β и не даёт ему взаимодействовать с рецептором на поверхности клетки
Несмотря на современные схемы лечения, у 25% людей, переживших инфаркт, в течение 5 последующих лет происходит ещё один случай инфаркта или инсульта, который пациенты часто не переживают. Причиной во многих случаях является воспалительный атеросклероз — образование бляшек на стенках сосудов, сопровождающееся воспалением.
Компания Novartis сообщила о первом успешном испытании по этому показанию препарата прямого противовоспалительного действия Canakinumab — антитела против интерлейкина-1-бета (IL-1β). IL-1β — белок, производимый активированными макрофагами в ходе развития воспалительной реакции, является одним из главных медиаторов воспаления, оказывает множественные эффекты на клетки иммунной системы и сосудов. Canakinumab связывается с IL-1β, не давая ему взаимодействовать со своими рецепторами, тем самым снижает воспаление, нормализует структуру стенки сосудов, и, в конечном итоге, приводит к снижению риска инфарктов и инсультов. Правда, как и всякий эффективный препарат, он имеет побочные действия, самым серьёзным из которых является повышение частоты инфекций — это логично, учитывая то, что воспалительная реакция как раз и является одной из линий защиты от болезнетворных микроорганизмов.
Исследование продолжалось более 6 лет и включило больше 10 000 пациентов. Теперь Novartis планирует обработать результаты исследования и подать документы на регистрацию по новому показанию.
Canakinumab уже зарегистрирован во многих странах (в том числе, в России под названием «Иларис») для лечения ряда воспалительных заболеваний — подагры, ювенильного артрита и некоторых других. Регистрация по профилактике повторных инфарктов и инсультов может значительно расширить сферу применения лекарства, так как, по некоторым оценкам, в 2015 году в мире произошло 7,29 млн инфарктов.
Ещё одно потенциально яркое событие в области кардиологии — успех CETP-ингибитора компании Merck & Co Anacetrapib. Это лекарство предназначено для профилактики не только повторных, но и первичных инфарктов у тех, кто принимает аторвастатин для снижения LDL-C (low-density lipoprotein, липопротеин низкой плотности, так называемый «плохой холестерин»). Такие пациенты подвержены повышенному риску сердечных проблем, и исследование на 30 000 людях показало значимое снижение риска по сравнению с группой плацебо.
CETP (Cholesteryl ester transfer protein — белок переноса эфиров холестерола) — белок плазмы, отвечающий за перенос эфиров и триглицеридов холестерола между липопротеинами. Было показано, что его ингибирование снижает LDL и повышает HDL (high-density lipoprotein, липопротеин высокой плотности). Казалось бы, это должно приводить к снижению смертности от сердечно-сосудистых заболеваний, которая ассоциирована с высоким уровнем LDL и низким HDL, однако на деле этого пока не удалось продемонстрировать. Это в очередной раз доказывает, что мы ещё очень слабо разбираемся в механизмах патологии сложных заболеваний и простые механистические подходы тут, как правило, не работают.
До опубликования полных результатов исследования многие относятся со скептицизмом к успеху Merck — очень необычным он выглядит на фоне многочисленных провалов других ингибиторов CETP в похожих исследованиях. Вполне может оказаться, что эффект статистически значим, но невелик, и тогда новому препарату не найдётся места на рынке. Также могут обнаружиться проблемы с безопасностью препарата, так как подобные молекулы склонны накапливаться в жировой ткани, вызывая побочные эффекты.
Успехи в лечении мигрени
Мигрень — третье по распространённости хроническое заболевание в мире, ей страдает около миллиарда человек. Существующие средства профилактики мигрени не помогают многим пациентам, а более половины отказываются от лечения из-за побочных эффектов.
В ближайшие годы ситуация в области профилактики мигрени может сильно измениться — положительные результаты ключевых исследований опубликовали сразу несколько компаний, занимающихся разработкой анти-CGRP препаратов, в том числе Teva, Eli Lilly, Alder, Amgen (у всех — антитела) и Allergan (малая молекула).
CGRP — пептид, который выделяется в волокнах тройничного нерва у пациентов, генетически предрасположенных к мигрени, и является сильнейшим вазодилататором (расширяющим сосуды веществом). Расширение сосудов приводит к местному отеку, привлечению в это место клеток, участвующих в процессе воспаления, высвобождению провоспалительных молекул. Это стимулирует болевые окончания мозговых оболочек, что приводит к дополнительной активации тройничного нерва, и порочный круг замыкается. Таким образом, снижение уровня CGRP или его рецептора играет важную роль в прерывании патологического процесса.
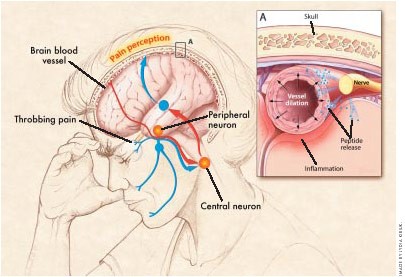 Рисунок 6. Схема развития мигрени. Выделение пептидов тканями нерва (синие точки) приводит к расширению сосуда и воспалению
Рисунок 6. Схема развития мигрени. Выделение пептидов тканями нерва (синие точки) приводит к расширению сосуда и воспалению
Ранее мы уже писали о некоторых из этих препаратов, когда они были на ранней стадии исследований. Теперь все они показали очень схожие результаты — у пациентов с 9—12 днями с мигренью в месяц число дней с мигренью снижается на 3—4, тогда как в группе плацебо на 1—2. Все новые препараты переносятся гораздо лучше, чем существующие противовоспалительные и триптаны. Конечно, полностью вылечить мигрень пока не удаётся, так как механизмы её возникновения слишком сложны и плохо изучены, но эти успехи — важный шаг вперёд в борьбе с болезнью.
Поскольку ни один из новых препаратов не сравнивался друг с другом напрямую, в одном исследовании, трудно сказать, какой из них лучше. Предположительно, они выйдут на рынок в следующем году, и маркетинговые отделы компаний ожидает жестокая конкуренция.
04.07.2017 Источник: 22century.ru