Моя улучшенная версия: как жить вечно

Джордж Чёрч [George Church] возвышается над большинством людей. У него длинная серая борода волшебника Средиземья, а работа всей его жизни – возиться с ДНК и копаться в секретах жизни – не так уж и далеко ушла от мира глубинной магии. 63-летний генетик заведует одной из крупнейших и хорошо финансируемых лабораторий мира, штаб-квартира которой находится на втором этаже массивного здания из стекла и стали, «Нового исследовательского здания» Гарвардской медицинской школы. Он также подрабатывает консультантом и осуществляет поддержку десятков проектов, консорциумов, конференций, подразделений и стартапов, объединённых миссией раздвигать границы доступного – от создания биороботов до воскрешения мамонта. Туманным августовским утром он захотел поговорить со мной о границах моей собственной жизни.
Чёрч – один из лидеров инициативы под названием «Проект геном-запись» (Genome Project-Write, GP-Write), организующей попытки сотен учёных всего мира, работающих над синтезом ДНК разных организмов. Группа всё ещё спорит по поводу того, как далеко следует заходить в вопросе синтеза человеческого ДНК, но Чёрч – стоя в своём офисе в мятой спортивной куртке за узкой кафедрой, которую он использует вместо стола – говорит, что его лаборатория уже сделала свой выбор по этому вопросу: «Мы хотим синтезировать модифицированные версии всех генов человеческого генома в следующие несколько лет».
Он собирается разработать и создать длинные цепочки человеческого ДНК, не просто вырезая и вставляя небольшие кусочки – подобная практика теперь сродни рутине, благодаря последним технологиям вроде CRISPR, позволяющим учёным дёшево и легко редактировать ДНК – но перезаписывая критически важные участки хромосом, которые затем можно соединить с геномом естественного происхождения. В случае успеха это будет захватывающий скачок по сложности от геномов бактерий и дрожжей, над синтезом которых учёные работали до сих пор. «Мы планируем вещи, намного превосходящие CRISPR,- говорит Чёрч. – Это похоже на разницу между редактированием книги и написанием новой».
При написании своей книги Чёрч надеется изменить в ней историю человека по своему желанию. Заменяя избранные нуклеотиды – символы жизни ACGT, разбросанные по хромосомам – и заменяя, допустим, T на А или С на G в процессе перекодирования, Чёрч мечтает создавать клетки, сопротивляющиеся вирусам. «Таким, как ВИЧ или гепатит Б», — говорит он.
«А простуде?» – спрашиваю я.
Он кивает, и добавляет, что они уже сумели перекодировать бактерию, сделав её невосприимчивой к вирусам. «Это описано в нашей работе от 2016 года», — говорит он.
Чёрч и другие, работающие над синтезом человеческого ДНК, создали свою собственный проект в рамках GP-Write – проект-запись человеческого генома (Human Genome Project-Write, HGP-Write). Его перспективы на успех таковы, что биологи с жаром обсуждают потенциал лечения болезней, создания клеток и даже, возможно, целых органов при помощи биоинженерии. Критики же задумчиво чешут головы из-за технических трудностей, высокой стоимости и вопросов практичности. Фрэнсис Коллинз, директор Национальных институтов здоровья, признаёт, что синтез полноценного человеческого генома реален, но ему непонятен смысл этой затеи. «Думаю, что это в пределах возможного, если у вас будет достаточно времени и денег, — говорит он, — но зачем это делать? Сегодня технологии вроде CRISPR гораздо более доступны».
А ещё встаёт вопрос этичности использования мощной технологии для игр с основным кодом жизни. Теоретически, учёные когда-нибудь смогут изготавливать геномы, человеческие или какие ещё, так же просто, как писать код на компьютере, превращая цифровые копии ДНК с чьего-то ноутбука в живые клетки или даже Homo sapiens. Памятуя о спорности ситуации, Чёрч и его коллеги по HGP-Write настаивают, что их целью является не создание новых людей – хотя одного лишь нахальства, необходимого для внесения широкомасштабных изменений в ДНК, достаточно, чтобы вызвать споры по этому поводу. «Люди расстраиваются, если кто-то размещает гены другого вида в еде», — говорит стэнфордский специалист по биоэтике и юриспруденции Генри Грили. «А тут речь идёт о полном переписывании жизни? Да тут волосы дыбом встанут, и это воспримут в штыки».
Но, несмотря на все штыки, Чёрч с командой рвутся вперёд. «Мы хотим начать с человеческой Y-хромосомы», — говорит он, имея в виду мужскую половую хромосому, у которой, как он поясняет, меньше всего генов из всех 23 хромосом, поэтому её легче всего создать. Но он не хочет синтезировать любую Y-хромосому. Они с командой хотят использовать последовательность этой хромосомы, взятую у реального человека – у меня.
«А вы можете это сделать?» – запинаясь, спрашиваю я.
«Конечно, можем – с вашего разрешения», — говорит он, напоминая, что моим геномом воспользоваться было бы легко, поскольку он хранится в цифровом виде в компьютерах его лаборатории, как часть проекта, запущенного им в 2005 году, «Проект персонального генома» (Personal Genome Project, PGP). PGP привлёк тысячи людей, согласившихся внести свой полный геном в открытую базу данных, доступную исследователям и вообще кому угодно; я тоже предоставил свой геном этому проекту.
С моего разрешения после нескольких нажатий клавиш на клавиатуре Чёрч без усилий сможет открыть цифровые чертежи моей Y-хромосомы. Затем учёные его лаборатории смогут сделать её синтетическую копию, но с отличиями: они перекодируют мою последовательность так, чтобы она сопротивлялась вирусам. Если им это удастся – и если они смогут перекодировать все остальные хромосомы и внедрить их в клетки человека, а это два больших «если» – теоретически, они смогут имплантировать эти «откорректированные» клетки мне в тело, где они, если повезёт, размножатся, изменят функционирование моего тела и понизят риск вирусной инфекции.
Но мы забегаем вперёд. Пока что Чёрч просто хочет перекодировать и синтезировать мою Y-хромосому. «Когда мы закончим, в холодильнике будет храниться маленькая частичка вас». Оптимизированная версия меня, которая однажды сможет оттаять – через десять лет, или через сотню тысяч. К тому времени, как говорит Чёрч, учёные смогут ещё глубже манипулировать моим геномом. Он смогут сделать меня сильнее, быстрее или даже умнее. Они, возможно, смогут создать совершенно новую версию меня. Кто знает, что станет возможным в будущем?
Синтетическая биология, область, посвящённая пониманию и переделке основных строительных блоков жизни, зародилась в 1970-х, когда команда под руководством стэнфордского биохимика Пола Берга совершила ключевые открытия в технике вырезания коротких последовательностей ДНК из одних организмов (от бактерий до людей) и вставки их в других (обычно бактерий). Эта практика позволила учёным использовать клеточные системы микробов для производства белков, которые в некоторых случаях стали успешными лекарствами, такими, как Epogen, использующийся для стимуляции производства красных кровяных телец у людей с анемией, проходящих процедуру диализа или участников Тур де Франс.
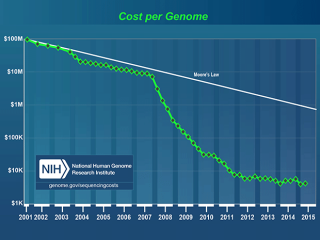
Крупномасштабная синтетическая биология начала появляться в начале 2000, когда учёные стали синтезировать вирусы целиком. В 2010 команда из института Дж. Крейга Вентера создала первую синтетическую самовоспроизводящуюся бактериальную клетку. Но пока ещё никто не приближался к амбициозным планам GP-Write или HGP-Write, обязанных своим именем изначальному проекту изучения человеческого генома Human Genome Project, массивного предприятия, в рамках которого было секвенировано 3 млрд пар генов, составляющих геном человека, за $2,7 млрд из денег налогоплательщиков США. (Второй, частный проект под руководством Крейга Вентера, сделал то же самое гораздо дешевле). «Мы считаем проект HGP-Write продолжением Human Genome Project», — сказал генетик Эндрю Хессел, один из основателей GP-Write и HGP-Write, и бывший исследователь в подразделении наук о жизни компании Autodesk.
Именно Хессел, стройный человек 54 лет, с короткой колючей бородкой, впервые рассказал мне об этом новом проекте изучения человеческого генома три года назад, когда я приезжал к нему в гости в его небольшой, броского вида коттедж рядом с Русской рекой в калифорнийском округе Сонома. Потягивая красное вино рядом с дровяной печкой туманным вечером, Хессел рассказывал, как начинал свою карьеру в конце 1990-х в Amgen, анализируя данные, полученные от частного проекта Вентера. «Ещё когда мы заканчивали HGP-Read (проект геном человека-чтение), — говорит он, используя их краткое обозначение проекта генома человека, — я уже предвкушал, как мы сможем начать что-то создавать. Я ждал и ждал, но ничего не происходило. Не хватало воображения. Технология дошла до определённой точки развития, но никто не двигался дальше». Он наблюдал за появлением CRISPR и других технологий редактирования генов, но они его не удовлетворили.
В 2015-м Хессел серьёзно решил заняться проектом редактирования генома и попросил Чёрча помочь организовать начинание, ставшее GP-Write (и HGP-Write). Чёрч настоял, что им необходимо привлечь ещё одного выдающегося специалиста по синтетической биологии, Джеффа Боэке из Нью-Йоркского университета. Цели группы простираются от помощи в разработке технологий, работающих быстрее и дешевле, до выработки этической платформы для синтеза жизни. У них уже есть ответ на вопрос Фрэнсиса Коллинза и прочих по поводу синтезирования генома человека – зачем это делать? Хессел, Чёрч и компания рассказывают о потенциале крупных изменений, затрагивающих весь геном целиком, которые можно использовать для разработки клеток, невосприимчивых к вирусам, синтетических органов и новых лекарств. Но они проводят черту, не активируя геном в клетках зародышевой линии, способных изменять гены, которые мы передаём нашим детям. «Мы не создаём младенцев – мы только редактируем геномы, — настаивает Хессел. – Реальная работа по созданию синтетического младенца останется следующему поколению».
В прошлом мае GP-Write провёл первую публичную встречу в Нью-Йоркском центре генома. Двухдневная конференция привлекла 250 учёных, специалистов по этике, юристов, учёных-любителей, художников, лиц, определяющих политику и компаний из 10 стран, включая Китай, Японию, Британию, Канаду, Сингапур и США. Там были доклады с названиями вроде «Использование изотермического увеличивающего массива для удлинения искусственной последовательности генов» или «Предсказание и понимание управляющих систем».
На конференции демонстрировались презентации опытных проектов, поддержку которых организация рассматривала или осуществляла. К примеру, Харрис Вон из Колумбийского университета хочет изменить клетки млекопитающих при помощи биоинженерии так, чтобы они стали фабриками по производству питательных веществ, выдавая критически важные аминокислоты и витамины, которые человеку приходится потреблять в виде еды. Ещё один проект от Джун Медфорд из Университета штата Колорадо направлен на редактирование геномов растений, которое позволит им заниматься фильтрованием воды или обнаружением химических веществ. На встрече она показывала изображение рамки аэропорта, окружённой распознающими взрывчатку кустами.
Движение GP-Write совершило самый новый из своих прорывов в прошлом году, когда лаборатория Боэке из Нью-Йоркского университета объявила о том, что полностью создала 6 искусственных хромосом из 16, составляющих геном дрожжей. Боэке планирует закончить синтез всех 16 хромосом к концу года. «Мы стремимся распутать, модернизировать и переделать генетические чертежи дрожжей, — говорит он. – После того, как мы синтезируем все 16 хромосом, мы планируем создать работающую клетку дрожжей».
Это будет примечательным достижением, но учитывая, что у дрожжей в четыре раза меньше генов, чем у людей, это вс ё равно не станет приближением к сложной задаче синтеза всего или даже части человеческого генома. Самые длинные из 16 хромосом дрожжей содержат примерно по миллиону спаренных оснований. Спаренное основание – это дублированные генетические буквы, идущие вдоль каждого отрезка двойной спирали ДНК, на манер ступеней лестницы. Y-хромосома содержит 59 млн спаренных оснований, и является одной из самых коротких хромосом из 23 человеческих. Некоторые учёные оценивают, что запись всего человеческого генома, всех 3 млрд спаренных оснований, может обойтись в $3 млрд, что не только нереально дорого, но и, возможно, и не нужно. «Нам не надо перезаписывать всё», чтобы серьёзно поменять хромосому, — поясняет Чёрч. – Только важные её части".
В 2002 году я, в рамках попыток нашего журнала объяснить и приблизить к народу новомодную технологию секвенирования генов, стал одним из первых людей, чей геном был секвенирован. Тогда мой геном казался чем-то очень личным, и обещал раскрыть секреты моего здоровья, погребённые глубоко в моей ДНК. В рамках подготовки статьи компания Sequenom проверила меня на несколько сотен маркеров ДНК, связанных с рисками заболеваний, от болезни Альцгеймера и повышенного кровяного давления до некоторых видов рака. К примеру, учёные из Sequenom обнаружили мутацию в моей шестой хромосоме, которую позже связали с небольшим увеличением риска сердечного приступа. Как и многие люди, геном которых секвенировали такие сервисы, как 23andMe, я запомнил эту информацию с пометочкой «хорошо об этом знать». Спустя пятнадцать лет и ноль сердечных приступов, я, разглядывая свой собственный проект HGP-Write, думал о том, как это – знать, что небольшая частичка меня копируется и перекодируются с целью улучшений.
После встречи с Чёрчем прошлым летом, я встретился с его командой в конференц-зале в гарвардском Вайссовском институте инженерного дела, вдохновлённого биологией, удивительном строении из стали и стекла, расположенном позади главного здания лаборатории Чёрча. В команде было четыре исследователя и постдок из Албании Эриона Хисолли 32-х лет. Очень серьёзная Хисолли, с косичками в волосах, провела меня по всей процедуре создания моей Y-хромосомы.
Синтез генов, объясняла Хисолли, начинается с того, что исследователи открывают генетическую последовательность на компьютере. На светящемся экране она показывает мне отрезок моей последовательности, который выглядит примерно так:
… и так далее. Хисолли поясняет, что, вместо синтеза каждого нуклеотида в моей Y-хромосоме, команда Черча сконцентрируется на отдельных единицах генетического кода, кодонах, определяющих, какую именно аминокислоту (и, в итоге, белок) будет производить клетка. Каждый кодон состоит максимум из трёх нуклеотидов (к примеру, ATG или TCC), и Хисолли с командой надеются, что, меняя местами определённые нуклеотиды в кодонах, они смогут произвести изменения в масштабе целого генома, способные сделать клетку устойчивой к вирусам. После перекодирования целевых кодонов, Хисолли отправит этот генетический чертёж в компанию Integrated DNA Technologies, производящую на заказ небольшие сегменты реальной ДНК, олигонуклеотиды. Затем компания высушит и заморозит эти олигонуклеотиды и отправит их обратно Хисолли. Они с коллегами будут соединять полученные отрезки во всё более длинные последовательности, и каждый новый сегмент будет на шаг приближать их к законченной хромосоме.
По крайней мере, такой план – и на его завершение может потребоваться целый год. А пока я прошу Хисолли провести менее амбициозную демонстрацию работы редактирования ДНК. Сначала она не хочет делать что-то, что считает простым. Но потом соглашается, и мы выбираем сегмент ДНК на моей шестой хромосоме, содержащий мутацию, выявленную моим предыдущим генетическим тестом – ту, что связана с небольшим риском сердечного приступа. Чтобы создать новую, улучшенную версию этого генетического фрагмента, Хисолли исправляет рискованную мутацию на компьютере. Она также перекодирует этот кусочек ДНК так, чтобы он сопротивлялся вирусам – просто для порядка. Потом Хисолли заказывает перекодированный фрагмент ДНК у компании, и тот через несколько дней спустя прибывает.
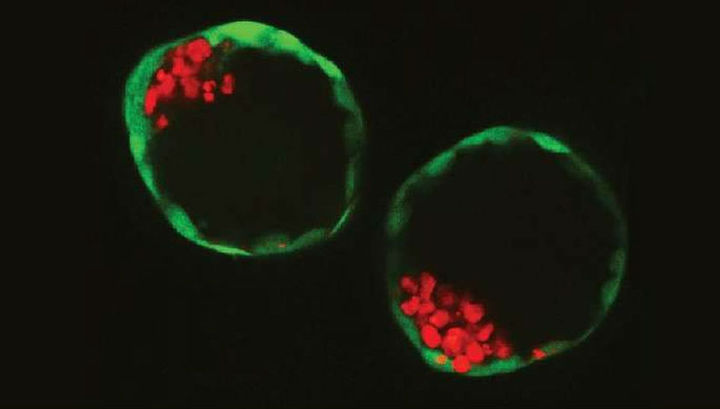
Получив фрагмент, исследователи клонируют его и помещают в цитоплазму E. coli, хорошо известной бактерии. Генетики часто пользуются способностью E. coli к быстрому размножению. Через несколько дней E. coli вырабатывает достаточное количество копий моей изменённой хромосомы, и Хисолли отправляет мне фото бактерий в чашке Петри, содержащих эти маленькие кусочки меня. Хотя я и не могу увидеть эти частицы наноразмера. Зато я могу увидеть разбросанные внутри клеток зелёные светящиеся капли. Эти капли воспроизводятся флуоресцентным репортёрным геном, взятым у медузы, который учёные постоянно используют для разметки генов. Этот грязноватый, коричнево-зелёный суп из микробов, покрытый светящимися пятнами, очень далеко отстоит от той версии меня, которую можно было бы узнать, но я скривился, представив, что однажды я смогу посмотреть на более полную версию моего генома в чашке Петри, карикатурно напоминающую меня.
Последний шаг в создании синтетического мини-меня – замена исправленного гена в тех клетках, где он должен храниться. Но не во всех – учёные используют мои белые кровяные тельца, чтобы создать индуцированные плюрипотентные стволовые клетки (ИПСК), способные вырасти и стать любой клеткой в моём теле. (Биоинженерной стороной вопроса занимается в Мэдисоне, штат Висконсин, компания Cellular Dynamics International, создающая стволовые клетки для фармацевтических компаний и институтов). Когда-нибудь эти клетки можно будет ввести в моё тело, в надежде, что они поменяют схему его работы, но пока что «поместить отредактированные клетки в тело – чрезвычайно трудная задача, — говорит Хисолли. – Во многие ткани можно просто ввести клетки напрямую и наблюдать, не сможет ли небольшой процент выжить и процветать. Или можно ввести кровяные стволовые клетки в вену и посмотреть, нацелятся ли они на костный мозг или тимус». И пока эта технология не разовьётся, мои отредактированные клетки будут храниться замороженными, чтобы в будущем к ним обратился я или кто другой.
Чёрч предупреждает, что технология масштабного синтеза генома всё ещё остаётся зарождающейся, дорогой и сложной. GP-Write ещё предстоит получить значимые инвестиции, хотя отдельные лаборатории, такие, как лаборатории Чёрча и Бокэке, получили финансирование от правительственных агентств, например, Национального научного фонда и DARPA, отделения Пентагона по исследованиям и разработкам. Пока что я не стал бы надеяться на то, что в ближайшее время смогу получить мою перекодированную Y-хромосому – или крохотное исправление, сделанное Хисолли в моей шестой хромосоме – в виде имплантата. Но они будут храниться в глубокой заморозке, на случай, если удастся разрешить массу этических и технических проблем, а также вопрос безопасности.
И всё-таки интересно, как в один прекрасный день можно будет использовать этот основной код, делающий меня тем, кто я есть. Я обеими руками за использование такой технологии для разработки новых лекарств или разработки подстроек ДНК на масштабе всего генома, способных предотвратить болезни, если это безопасно и не несёт в себе намеренных отрицательных эффектов – и это очень большое «если». Но если мы преодолеем терапевтический барьер, интересно, как отнесусь к тому, что я, или мои дети, будут улучшены и станут сильнее или умнее. Повторюсь, что если это безопасно и на самом деле сработает, то подозреваю, что множество людей с готовностью согласятся на апгрейд, хотя приходится задуматься, не приведёт ли появление новых, улучшенных геномов – будем мы использовать перекодирование в масштабе генома или технологии, подобные CRISPR – к тому, что мы полностью изменимся.
Чем это обернётся в ближайшие годы и десятилетия – остаётся только догадываться. Но прямо сейчас уже изготавливаются инструменты, которые смогут дать нам возможность делать нечто большее, чем просто вводить несколько новых улучшений, говорит биоинженер Пэм Сильвер из Гарварда: «Ограничивать вас будет только ваше воображение». Она работает в проекте GP-Write, направленном на изготовление аминокислот, которые люди получают с едой. Её мнение поддерживает генетик Чарльз Кантор, почётный профессор из Бостонского Университета, помогавший мне участвовать в секвенировании моей ДНК в 2002-м в Sequenom. Кантор считает, что учёные и специалисты по этике слишком робкие. «Когда я представляю себе редактирование генома, — говорит он, — мне нравится думать о том, в каких разных жанрах люди могут писать сочинения. Лично мне нравится беллетристика – придумывать совершенно новые геномы, например, создавать людей, получающих энергию из фотосинтеза или шагающие растения».
То, что исследователи уже всерьёз думают о клетках, способных сопротивляться вирусам или ходящих растениях, делает ещё более важной необходимость для учёных, таких, как Чёрч, Хессел и Боэке, а также молодых исследователей вроде Хисолли, рассказывать о своей работе публично, а для передовых проектов вроде GP-Write – работать прозрачно и по возможности придерживаться стандартов. «Думаю, что общественность должно успокоить, что учёные об этом задумываются, а не просто берут и делают что-то из разряда безумного гения», — говорит Николь Локхарт, директор программы Национальных институтов здоровья по исследованию этических, юридических и социальных последствий. Или, как говорит Хессел: «Может, мы и не сумеем предотвратить использование этой технологии плохими парнями, но поскольку она так или иначе появится, всегда лучше открыто говорить об этом».
Во время одного из последних визитов в лабораторию я спросил у Хисоли, какую хромосому они будут испытывать в следующий раз, когда закончат синтезировать мою Y.
«Мы пока не знаем», — говорит она. Возможно, одну из оставшихся малых хромосом, 21 или 22. Чёрч побуждает её и её команду попытать шансы с X-хромосомой.
«Но на данный момент это будет немного чересчур», — говорит Хисолли, учитывая, что в ней более чем в 10 раз больше генов, и что она гораздо больше, чем Y.
Я осторожно спрашиваю её, чью последовательность они будут использовать в случае с этой и остальными хромосомами для создания остатках перекодированного искусственного генома человека.
«Мы могли бы использовать вашу», — говорит она, едва-едва улыбаясь мне перед тем, как отвернуться и продолжить работу.
05.05.2018 Источник: geektimes.com