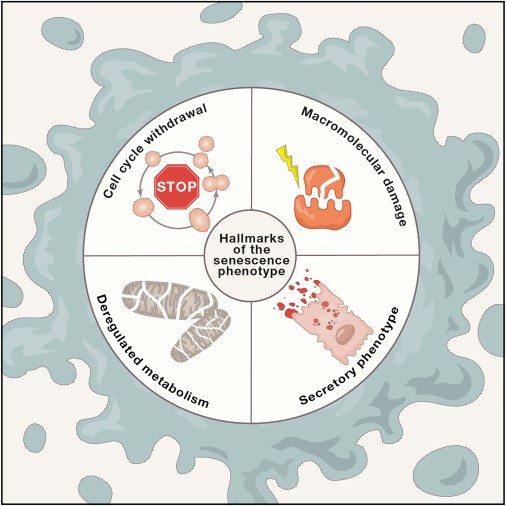
Старение: запрограммированный процесс, который можно прервать, или неизбежность?

Новость о том, что в Москву прилетел Мартин Макфлай — герой ставшего легендарным сериала «Назад в будущее» — взорвала все социальные сети, а у многих навернулись ностальгические слезы, потому что с этого года все события, описанные в фильме, происходят в прошлом. «Время не повернуть вспять» — расхожее выражение, но мечты об осуществлении этой идеи не оставляют в покое лучшие умы человечества. Течение времени подразумевает, увы, старение, и ученые пытаются направить стрелки «биологических часов» вспять или хотя бы замедлить их ход.
На страницах истории нередко встречаются попытки создания эликсира молодости. Ходили слухи о том, что, например, Казанова принимал это зелье и на протяжении многих лет сохранял молодость и красоту. Сейчас проблема старения рассматривается намного шире: речь идет не только о старении внешнем (морщины, физическая слабость), а о причинах и молекулярных механизмах, связанных с этим процессом; ведутся горячие споры между двумя лагерями ученых, которые удачно названы В.П. Скулачёвым «пессимистами» и «оптимистами». Первые говорят о том, что старение неизбежно, этот процесс подобен тому, как изнашиваются механизмы машины, и ничего не остается, как выкинуть ее на свалку. «Оптимисты» же говорят нам о том, что старение вполне можно остановить, потому что это программа, работу которой можно нарушить*.
* — Оптимисты из оптимистов, в частности, трансгуманисты, вообще настаивают на том, что старение — это болезнь, и что за ее лечение всерьез необходимо взяться всем миром. — Ред.
Предполагаемые «часы» старения
Говоря о возможных механизмах старения, часто упоминают так называемые «часы» старения. Не утихают споры о том, по каким же из них нам нужно сверять время. В таблице ниже приведено множество кандидатов на роль «часов» старения.
Таблица 1. Кандидаты на роль «часов» старения. Таблица из [4].
| Предполагаемые «часы» старения |
Теория, гипотеза |
| ДНК |
Теории «катастрофы ошибок» и накопления спонтанных мутаций |
| Макромолекулы |
Теория «сшивок» |
| Митохондрии |
Свободнорадикальная теория |
| Клетка |
«Лимит Хейфлика» (теломерная теория) |
| Половые железы |
Инволюция половой функции |
| Надпочечники |
Снижение продукции дегидроэпиандростерона |
| Щитовидная железа |
«Гормон смерти» Доннера Денклы |
| Иммунная система |
Иммуностарение |
| Гипоталамус |
Нейроэндокринные теории |
| Эпифиз |
Мелатонин как счетчик внутреннего времени в солнечных часах старения |
Есть идея о существовании общего прообраза «биологических часов» — группы ферментов под названием пероксиредоксины, которые участвуют в утилизации токсичной перекиси водорода — побочного продукта кислородного дыхания. Как оказалось, пероксиредоксин в эритроцитах человека и в морских водорослях переходит из окисленной в восстановленную форму каждые 24 часа. Это наводит на мысль, что он имеет отношение к циркадным ритмам, которые у человека регулируются эпифизом, одним из кандидатов на роль «часов» старения. Так вот, есть предположение, что пероксиредоксин — это «прапрадедушка» всех биологических «часов». Эта система появилась 2,5 млрд лет назад, когда на планете зародились фотосинтезирующие организмы, изменившие характер атмосферы с восстановительного на окислительный (это событие известно под названием «кислородной катастрофы») [1]. Но пока это гипотетические часы, которые нужно тщательно разобрать на все винтики и шестеренки.
Другой вопрос: а можно ли ход подобных «часов» повернуть вспять? Есть несколько идей, как можно это сделать — пока на животных и культурах клеток:
- Создать «молодое окружение» (опыты по гетерохроническому парабиозу — например, сшиванию боками молодой и старой крысы, при котором старое животное «омолаживается»).
- Воздействовать на работу определенных генов (например, NFκB — транскрипционного фактора, регулирующего гены иммунного ответа, клеточного цикла и апоптоза).
- Воздействовать фармакологическими препаратами на клетки (например, рапамицином — ингибитором mTOR, ферментом — сенсором уровня питательных веществ в клетке, регулирующим синтез белков. При введении рапамицина старым мышам продолжительность их жизни возрастала, увеличивалась и пролиферация стволовых клеток) [2].
Гены старения и долголетия
Ладно, скажете вы, ну а что же с генами-то? Терпение, дорогой читатель! Воистину чудотворный эксперимент с продлением жизни растения резушки (на профессиональном языке — арабидопсиса) был проведен научной группой Зигберта Мельцера. Но сначала хочется сказать пару слов об этом замечательном растении. Дело в том, что оно является излюбленным объектом генетиков (как кишечная палочка у молекулярных биологов или крыса у физиологов), так как жизненный цикл арабидопсиса настолько короток, что его можно пронаблюдать целиком за время одного чемпионата по футболу. Это наводит на мысль о том, что существует программа, которая запускает гибель арабидопсиса после его цветения и размножения. Так вот, Мельцеру и соавторам удалось «сломать» эту программу, но, как это часто происходит в науке, случайно. Был создан генетически модифицированный арабидопсис с двумя «выключенными» генами, что привело к увеличению продолжительности жизни растения в девять раз [3]!
Теперь поговорим о «генах старения» у червей. Ген age-1 был найден у еще одного любимого объекта биологов — нематоды Caenorhabditis elegans. Оказалось, что при нокауте age-1, отвечающего за работу фермента PI3-киназы, продолжительность жизни этого прозрачного червячка возрастает в 2 раза! Интересно, что у нематоды был найден ген daf-2, гомологичный гену рецептора инсулина, и уменьшение его активности тоже приводит к двукратному продлению жизни. Считается, что одна из причин замедления старения Caenorhabditis elegans при выключении описанных выше генов — это замедление основного обмена нематоды. Удивительно то, что здесь можно провести параллель и с нами: предполагается, что старение можно замедлить, сократив потребление калорийной пищи — то есть опять-таки снизив уровень метаболизма [3, 4]. Вот и задумаешься: может, не ходить на работу, впасть в анабиоз и поменьше есть?..
А вот плодовая мушка Drosophila melanogaster, именем которой с легкой руки советского генетика Тимофеева-Ресовского когда-то был назван научный кружок генетиков — «Совместный ор дрозофиле» (Дрозсоор). Чем же интересна эта мушка? Оказалось, что на дрозофиле тоже удобно изучать процессы старения и долголетия. Была получена линия мух с мутацией в гене Сu,Zn-супероксиддисмутазы (СОД) — фермента, который уменьшает количество свободных радикалов в клетке. У таких дрозофил продолжительность жизни заметно падала по сравнению с диким типом, и была отмечена повышенная чувствительность к веществам, продуцирующим свободные радикалы. С другой стороны, у мух с увеличенным числом копий генов Сu,Zn-СОД и каталазы (фермента, запускающего реакцию разложения перекиси водорода на молекулярный кислород и водород) продолжительность жизни возрастала, но только в том случае, если умножалось число копий генов обоих ферментов. И снова вспомним о системе передачи сигнала от инсулина и инсулинопободного фактора роста 1 (ИФР-1), которые, как и у нематоды, регулируют продолжительность жизни. Мутации в регуляторном участке гомолога гена рецептора инсулина (chiko) продлевают плодовым мушкам жизнь на 45% [4].
Найдены «гены старения» и у млекопитающих — например, у карликовых мышей Эймса с мутацией в гене транскрипционного фактора Prophet of Pit-1 (Prop-1). Живут такие мыши на 50% дольше своих диких сородичей, но, увы, им приходится расплачиваться за это нарушением гормонального фона (у них снижены уровни тиреотропного гормона (ТТГ), пролактина, ИФР-1) и карликовостью. У линии мышей Snell c мутацией в гене Pit-1 (транскрипционного фактора, регулирующего дифференцировку тех клеток гипофиза, которые выделяют пролактин и гормон роста) продолжительность жизни тоже выше, чем у обычных мышей. Однако, как и мыши Эймса, они карликовые — из-за недостаточного выделения гормона роста [3, 4].
Говоря о генах старения и долголетия, автор неоднократно упоминает об инсулине, и это неспроста: этот гормон является очень важным регулятором метаболизма и, как выяснилось, долголетия у дрозофилы, нематоды и мыши (и не только у них), которые друг другу «седьмая вода на киселе» в эволюционном смысле этих слов. На рисунке 1 представлено сравнение сигнальных путей инсулина и ИФР-1 у этих организмов.
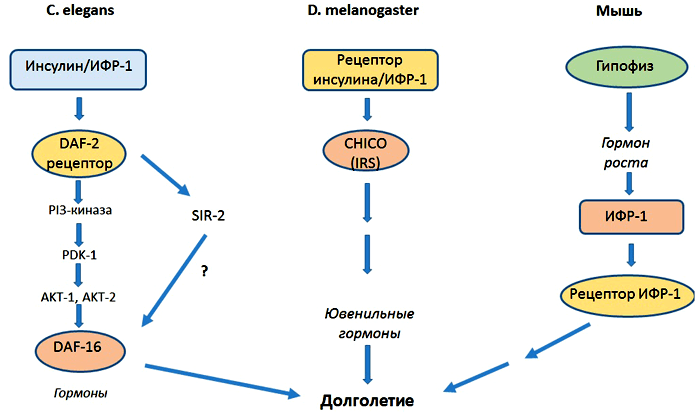 Рисунок 1. Схема передачи инсулинового сигнала у нематоды, плодовых мух и млекопитающих. Рисунок из [4].
Рисунок 1. Схема передачи инсулинового сигнала у нематоды, плодовых мух и млекопитающих. Рисунок из [4].
«Ну и что? Черви, мушки, мыши... А что же с нами?» — спросите вы, дорогие читатели. Что касается нас, то многие геронтологи подчеркивают особое значение для долголетия гена аполипопротеина Е (ApoE) — белка, играющего важную роль в транспорте и метаболизме жиров. У людей распространены три аллеля этого гена — ε2, ε3, и ε4, различающиеся всего парой нуклеотидных замен. Бόльшая часть населения имеет «нейтральный» аллель ε3, который не связывают с развитием каких-то патологий. Но интересно, что в популяции долгожителей (80-100-летних людей) повышается доля аллеля APOE ε2, а ε4, наоборот, значительно сокращается. Это может свидетельствовать о благоприятном влиянии первого варианта на здоровье и продолжительность жизни и о тенденции к ранней гибели носителей второго варианта (ε4 раньше элиминируется из популяции). Подкрепляет такое предположение ряд исследований, выявивших, что аллель ε4 увеличивает риск раннего развития атеросклероза и ишемической болезни сердца, а также болезни Альцгеймера [4].
«Я вся такая противоречивая!» Про белки апоптоза и активные формы кислорода
«Лучше меньше, да лучше», «Семь раз отмерь — один раз отрежь» — все эти пословицы говорят о том, что нужно работать вдумчиво и внимательно, лучше сделать меньше, но качественнее. Но... не все следуют народным мудростям, тем более -ферменты. В наших клетках есть энергетические станции — митохондрии, которые работают не покладая рук, а точнее, белков-ферментов дыхательной цепи — бравых молодцов, которые без устали окисляют жиры и углеводы, добывая энергию. Но работают они, скажем так, не совсем «чисто»: в процессе окисления образуются довольно вредные соединения — активные формы кислорода (АФК), которые окисляют липиды клеточных мембран и белки. Повышенное содержание АФК может спровоцировать перерождение нормальной клетки в раковую.
Чтобы не дожидаться такого печального события, клетка может сама себе сделать «харакири», то есть запустить процесс апоптоза. Но неужели АФК настолько плохие и приносят нам только вред? Нет! Не зря Маяковский писал: «Послушайте! Если звезды зажигают, значит, это кому-нибудь нужно?» Нужно! Если совсем убрать АФК, это тоже не приведет ни к чему хорошему. Показано, что небольшие их концентрации необходимы для процессов дифференцировки стволовых клеток в специализированные клетки соответствующих тканей. А высокие концентрации АФК используются фагоцитами как «биологическое оружие» для борьбы с патогенами [3]. Еще один совсем недавно открытый эффект — участие АФК в регуляции процессов, лежащих в основе обучения и памяти. Как известно, основная функция нервных клеток — получать и передавать электрические сигналы посредством межклеточных контактов — синапсов. Именно здесь определяется, будет ли входящий с другого нейрона электрический сигнал передан дальше следующим нейронам, или же он пропадет бесследно. При этом мозг — динамичная структура, и проводимость самих синапсов может меняться. На клеточных культурах, а потом и в исследованиях на модельных животных было показано, что активные формы кислорода просто необходимы для регулирования проводимости синапсов [5]. Так что АФК — это коварный двуликий Янус.
Вопрос жизни и смерти. Бифункциональные белки
Теперь вернемся к вопросу об апоптозе. На первый взгляд кажется, что белки, запускающие апоптоз, исключительно вредны — ну какая от них может быть польза, если они запускают клеточную смерть? Но это не совсем так. Есть так называемые бифункциональные белки, которые, как понятно из их названия, выполняют разные функции в клетке, связанные с ее жизнью и смертью (рис. 2). Например, цитохром с участвует в запуске апоптоза: он выходит из митохондрии и взаимодействует с белком Apaf-1 в цитоплазме. С другой стороны, он участвует в переносе электронов по дыхательной цепи митохондрий, что, несомненно, является его положительной функцией. Найдена альтернативная, «хорошая» функция и белка Apaf-1: он участвует в процессах остановки клеточного деления в случае повреждения ДНК. При этом белок перемещается из цитоплазмы в ядро и взаимодействует с чекпойнт-киназой 1 (Chk1). Однако и апоптоз иногда — событие желательное, поэтому однозначно неприятельскими действия его стимуляторов тоже нельзя назвать.
 Рисунок 2. На наших глазах разыгрывается шекспировская трагедия в современном прочтении: клетке предстоит разобраться, уйдет она в апоптоз или нет. Ведь белки, которые она держит в руках, бифункциональные.
Рисунок 2. На наших глазах разыгрывается шекспировская трагедия в современном прочтении: клетке предстоит разобраться, уйдет она в апоптоз или нет. Ведь белки, которые она держит в руках, бифункциональные.
А вот другой интересный бифункциональный белок — Cdc6. Он препятствует сборке апоптосомы — структуры, необходимой для начала апоптоза, — взаимодействуя с Apaf-1. Другая функция Cdc6 — участие в репликации хромосом и стимуляции пролиферации клеток. Парадокс заключается в том, что и ген APAF1, и ген CDC6 активируются одним и тем же транскрипционным фактором, E2F [6]. Еще один белок апоптотического каскада — каспаза-9. Помимо участия в программируемой клеточной смерти, она необходима для дифференцировки стволовых клеток в мышечные [3].
У растений тоже похожая ситуация с вопросами жизни и смерти: фитогормон абсцизовая кислота, вызывающий гибель однолетних растений, еще и регулирует развитие зародыша, размножение, деление клеток и защиту от стресса [3].
Лекарство от старости
Говорим о лекарстве от старости — подразумеваем ион Скулачёва (см. врезку ниже) [7]. Остановимся на этом подробнее. SkQ1 — это молекула-«электровоз» с «прицепом» в виде антиоксиданта, которая идет по маршруту до конечной станции «митохондрия». Было показано, что SkQ1 способен проникать через биологические и искусственные мембраны, доставляя антиоксидант именно в митохондрии, и при этом ион спасал клетки от апоптоза, вызываемого свободными радикалами. В итоге SkQ1 стал основой для создания лекарств от старости. Первым препаратом стал «Визомитин» — глазные капли, которые лечат синдром «сухого глаза». А начиналось всё с того, что в ходе серий экспериментов удалось вернуть зрение кошкам, собакам, лошадям, ослепшим из-за старости. Конечно же, лечение синдрома «сухого глаза» — это не предел, и хочется верить в то, что позже будут созданы и другие препараты, лечащие заболевания, связанные с патологией митохондрий.
Говорим о лекарстве от старости — подразумеваем ион Скулачёва
И так происходит благодаря особому отношению популярных изданий и телеканалов к этой субстанции. Поэтому стоит хоть немного (и без эмоций) разобраться с научной составляющей изобретения. Каким образом должны действовать эти молекулы и действуют ли?
Во-первых, при каких состояниях и в каких обстоятельствах они эффективны (по заявлению разработчиков), и как это подтверждено, можно самостоятельно изучить по материалам, представленным на сайтах Проект «Ионы Скулаёва» и Глазные капли «Визомитин».
А во-вторых... Что касается старения, то базисом для веры в эффективность субстанции SkQ1 будет принятие человеком тезиса, что старение — процесс запрограммированный (обусловленный необходимостью очищать пространство для молодых, размножающихся, творящих эволюцию), но главное — реализуемый вполне определенными «киллерами» — свободными радикалами. Значит, достаточно нанять киллера для ликвидации этого киллера — и жить будем если не дольше, то счастливее. Если такой теоретический базис у кого-то не вызывает отторжения или сомнений, хорошо. Идём дальше.
«Киллер киллера» устроен, действительно, очень разумно и красиво. Паровоз — ион (катион) Скулачёва (Sk) + крепление — линкер из алифатического углеводорода + вагон — главный исполнитель, антиоксидант. Вариантов всех трех компонентов перепробовали много. Сейчас «продвигается» в основном одна комбинация — SkQ1, состоящая из трифенилфосфония (липофильный катион, легко преодолевающий мембраны клетки и митохондрии, чтобы достичь наиболее отрицательно заряженного митохондриального матрикса), декана (обеспечивает правильное позиционирование антиоксидантного «вагона» в мембране митохондрии) и пластохинона (антиоксиданта из хлоропластов). Эффект должен опосредоваться прямым уничтожением АФК за счет окисления пластохинона и снижением мембранного потенциала (здесь работает даже катион без антиоксиданта). Достоинство такого комплекса: целенаправленная борьба с АФК прямо в месте их образования (митохондриальной ЭТЦ), быстрое восстановление «использованного» пластохинона, большой люфт между дозами, обеспечивающими нейтрализацию радикалов и оказывающими прооксидантный эффект (да, увы, для антиоксидантов характерна такая подлость).
Итак, конфигурация красивая и остроумная, in vitro работает. А что же в сухом медицинском остатке? (Ведь именно это должно поднять нас на другой уровень относительно простой веры в теорию «феноптоза» — с его карающим мечом в виде АФК (по Скулачёву) — и научную красоту разработки.) На рынок помимо ветеринарных глазных капель вышел пока единственный SkQ1-содержащий препарат — «человеческие» глазные капли «Визомитин» (пластохинонилдецилтрифенилфосфония бромид). Клинические исследования они проходили как препарат для лечения синдрома «сухого глаза» (так проще и быстрее). В испытании (контролируемом, но «не слепом», судя по всему) «Визомитином» лечились 20 человек, другим препаратом из категории «искусственных слёз» — ещё 20. По некоторым параметрам SkQ1-капли показали лучший результат. Напомним, что клинические испытания в идеале не должны завершаться после первой фазы, где оценивается в основном безопасность препарата, обратим внимание и на дизайн (размер выборок, возможность предвзятости, если испытание «не слепое»). Но теперь препарат можно купить в аптеке и... поучаствовать в дальнейших испытаниях, уже за свой счет. Либо повременить с покупкой до завершения начавшегося пострегистрационного международного многоцентрового двойного слепого рандомизированного плацебо-контролируемого клинического исследования, купив что-нибудь не такое наукоёмкое, но дешевое и для увлажнения глаз вполне достаточное. А оценить эффективность именно «тяжелой артиллерии» — митохондриально-направленного антиоксиданта — можно будет после появления результатов испытаний (двойных слепых рандомизированных плацебо-контролируемых, как указано на сайте «Визомитина», уже завершенных) по терапии катаракты и глаукомы. Планируются масштабные исследования и по возрастной макулярной дистрофии.
Ну а модуляция старения организма — тема уж слишком перспективная. Пока только пробирки, грызуны, рачки и мушки. Удалось, например, повысить среднюю, но не максимальную продолжительность жизни мышей, то есть гораздо больше мышей в выборке дотягивало до «отведенного» — стандартного для этой линии грызунов — срока, но сам срок особо не отодвигался. Есть некоторые успехи и в других направлениях. Людям же еще долго придется обходиться без SkQ1-геропротекторов. Так что называть эту разработку «лекарством от старости» по меньшей мере преждевременно.
Редакция.
ПОДРОБНЫЙ ОБЗОР ЛЕКАРСТВ ОТ СТАРОСТИ ИЩИТЕ ЗДЕСЬ: ГЕРОПРОТЕКТОРЫ
«Главное, ребята, митохондриями не стареть!» Нестареющие животные
Пожалуй, в свете свободнорадикальной теории старения, именно так стόит петь слова из известной песни. Одним из выдающихся примеров незначительно стареющих животных является голый землекоп, Heterocephalus glaber. Разгадать секрет долголетия этого животного пока не удалось. Как выяснилось, землекопы обычно погибают от причин, не связанных со старением: в первые месяцы жизни, критичные для «младенцев» большинства животных, или в результате стычек с родственниками и соседними кланами землекопов. А «царица» и ее «мужья» — у землекопов матриархат — вообще изолированы от внешних опасностей, и в естественных условиях продолжительность их жизни по сравнению с другими членами популяции самая высокая. Но вот создается впечатление, что старение митохондрий — это вообще не про землекопа! В лаборатории Рошель Баффенстайн было показано, что при добавлении АФК к культуре клеток землекопа клетки... не уходят в апоптоз! То есть, если считать, что АФК реализуют программу старения*, у землекопа эта программа отключена за ненадобностью [3].
* — А если так не считать, всё может встать на свои места. Старая добрая свободнорадикальная теория, особенно в исходном виде и «единолично», вряд ли может объяснить феномен старения (и особенно старения пренебрежимого). Тем более что землекопы — великие мастера апоптоза, просто это с АФК у них не связано: их клетки организованно самоуничтожаются в нужный момент, предотвращая этим гибель целого организма. Детально мы рассмотрим причудливые защитные механизмы голого землекопа в одной из статей цикла, посвященного старению и борьбе с ним. В цикле вскользь будут затронуты и основные теории старения, уже сейчас можно познакомиться с эпигенетической концепцией («Старение и долголетие: эпигеном раскрывает тайны») [8] и поразмыслить над связью клеточного старения с организменным («Зачем клетки стареют») [9]. В обеих статьях есть информация по АФК, а в последней — и по землекопу. — Ред.
Другое нестареющее млекопитающее — это гренландский кит. Известно, что эти киты выбрасываются на берег и из-за этого, увы, погибают. Сейчас появилось предположение, почему же они это делают. Возможно, киты... слепнут: у них развивается катаракта. Здесь речь идет об исключительно химическом старении. Дело в том, что в хрусталике кита идет спонтанная L→D-изомеризация белка кристаллина. В итоге получается, что у 200-летнего животного 40% L-аспартата превращается в D-изомер, что может вызывать помутнение хрусталика [3].
НОВОСТИ О НЕСТАРЕЮЩИХ ЖИВОТНЫХ ЧИТАЙТЕ ЗДЕСЬ: ЖИВОТНЫЕ ДОЛГОЖИТЕЛИ
Антиоксиданты и молекулярная косметология
...что есть красота
И почему ее обожествляют люди?
Сосуд она, в котором пустота,
Или огонь, мерцающий в сосуде?
Н. Заболоцкий. Некрасивая девочка
Всем хочется быть красивыми и не стареть. Лет 20 назад начался настоящий бум на рынке косметических средств, рекламирующих антиоксиданты как панацею в борьбе со всеми проявлениями старения. Известно огромное количество антиоксидантов, которые борются с АФК, в том числе и природных: это витамины Е и С, коэнзим Q, флавоноиды зеленого чая. К синтетическим относятся N-ацетилцистеин, идебенон, тролокс и другие. До сих пор мы сталкиваемся с тем, что полки магазинов завалены косметическими чудо-средствами, которые напичканы спасительными антиоксидантами. Часть из этих мифов приходится развеивать, но, к счастью, некоторые их них при внимательном рассмотрении из мифов превращаются в реальность. Например, тот факт, что антиоксиданты могут замедлять старение кожи (рис. 3), — правда. Вопрос только в том, как их туда (под верхние слои эпидермиса) правильно доставить. Есть интересное исследование, проведенное на культуре кератиноцитов — основных клеток эпидермиса. При обработке этих клеток коктейлем из антиоксидантов (коэнзим Q, масло криля, липоевая кислота, масло виноградной косточки, α-токоферол) в присутствии фактора некроза опухоли альфа (ФНО-α) в них значительно снижалось содержание NFκB. То есть, проще говоря, клетки, обработанные этими антиоксидантами, были больше защищены от запрограммированной клеточной гибели, чем контрольные кератиноциты, не обработанные ими. Эта работа подтверждает тот факт, что антиоксиданты действительно можно и нужно использовать в косметических средствах, направленных на борьбу с возрастными изменениями кожи [10]. Но повторимся: другой вопрос — как их туда доставить?
 Рисунок 3. Процесс старения кожи. Рисунок с сайта ladyk.by.
Рисунок 3. Процесс старения кожи. Рисунок с сайта ladyk.by.
Что же касается мифов, то перед покупкой очередного чудо-средства стόит задуматься над следующими вещами:
- условиями хранения таких косметических средств;
- концентрацией активного вещества;
- а пройдут ли эти активные вещества вообще через кожный покров?
После этого постоять, подумать возле витрины, покрутить в руках чудо-баночку... и, увы, в большинстве случаев поставить ее обратно на полочку.
Заключение
Выясняя работу часов старения, ученым порой приходится быть слепыми часовщиками: сложно понять механизм вслепую, но при желании шаг за шагом можно нащупать новые детали и понять, как они взаимодействуют друг с другом.
Ссылки на источники находятся в оригинале статьи: biomolecula.ru